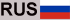Im Gehirn erscheint weiterhin ein Protein namens Reelin, das dem Altern und der Alzheimer-Krankheit entgegenwirkt. Ein Protein, das die Bildung des Gehirns in jungen Jahren unterstützt, scheint das Organ auch vor der Alzheimer-Krankheit und anderen altersbedingten Krankheiten zu schützen. Japanische und europäische Neurowissenschaftler haben herausgefunden, dass die Einführung großer Mengen Dopamin in die Gehirne von Mäusen, die für die Entwicklung der Alzheimer-Krankheit prädisponiert sind, zu einer beschleunigten Produktion des Enzyms führt, das für die Zerstörung pathogener Beta-Amyloid-Proteinmoleküle verantwortlich ist.
Drei im letzten Jahr veröffentlichte Studien deuten darauf hin, dass das Protein Reelin das Denken und Gedächtnis in erkrankten Gehirnen unterstützt, obwohl unklar bleibt, wie genau es dies tut. Untersuchungen zeigen auch, dass Neuronen anfälliger werden, wenn der Reelin-Spiegel sinkt.
Laut Li-Hui Tsai, Professorin am MIT und Direktorin des Picower Institute for Learning and Memory, gibt es zunehmend Hinweise darauf, dass Reelin als „Schutzfaktor“ im Gehirn wirkt.
„Ich denke, wir kommen etwas Wichtigem im Kampf gegen die Alzheimer-Krankheit näher“, sagt Tsai.
Die Forschung hat die Entwicklung eines Medikaments inspiriert, das den Reelin-Spiegel erhöht oder ihnen hilft, besser zu funktionieren, um einem kognitiven Verfall vorzubeugen.
„Man muss kein Genie sein, um zu sagen: ‚Mehr Reelin, das ist die Lösung‘“, sagt Dr. Joseph Arboleda-Velazquez von der Harvard Medical School und der Massachusetts Eye and Ear Infirmary. „Und jetzt haben wir die Werkzeuge dafür.“
Im Jahr 2023 erlangte das Protein Reelin dank einer Studie am Gehirn eines kolumbianischen Mannes, bei dem erwartet wurde, dass er im mittleren Alter an Alzheimer erkrankt, dies aber nicht der Fall war, so etwas wie eine wissenschaftliche Berühmtheit.
Der Mann, der als Mechaniker arbeitete, gehörte zu einer großen Familie, die eine sehr seltene Genvariante namens Paisa trägt, eine Anspielung auf die Gegend um Medellin, wo sie entdeckt wurde. Familienmitglieder, die diese Variante erben, werden mit ziemlicher Sicherheit im mittleren Alter an Alzheimer erkranken.
„Mit 40 beginnen sie einen kognitiven Verfall zu erleben und entwickeln dann in ihren späten Vierzigern oder frühen Fünfzigern eine ausgewachsene Demenz“, sagt Arboleda-Velázquez.
Allerdings behielt dieser Mann trotz dieser Variante seine kognitiven Fähigkeiten bis zum Ende seiner Sechziger und bei ihm wurde erst im Alter von 70 Jahren Demenz diagnostiziert.
Nach seinem Tod im Alter von 74 Jahren ergab eine Autopsie, dass das Gehirn des Mannes mit klebrigen Amyloid-Plaques übersät war, einem Kennzeichen der Alzheimer-Krankheit.
Wissenschaftler haben außerdem ein weiteres Kennzeichen der Alzheimer-Krankheit entdeckt: verknotete Fasern namens Tau, die Neuronen schädigen können. Überraschenderweise fehlten diese Knäuel jedoch größtenteils in einer Region des Gehirns, die als entorhinaler Kortex bezeichnet wird und an der Erinnerung beteiligt ist.
„Das ist wichtig, da dieser Bereich normalerweise einer der ersten Bereiche ist, die von der Alzheimer-Krankheit betroffen sind“, sagt Arboleda-Velazquez.
Forscher haben das Genom des Mannes untersucht. Und sie entdeckten etwas, das erklären könnte, warum sein Gehirn geschützt war.
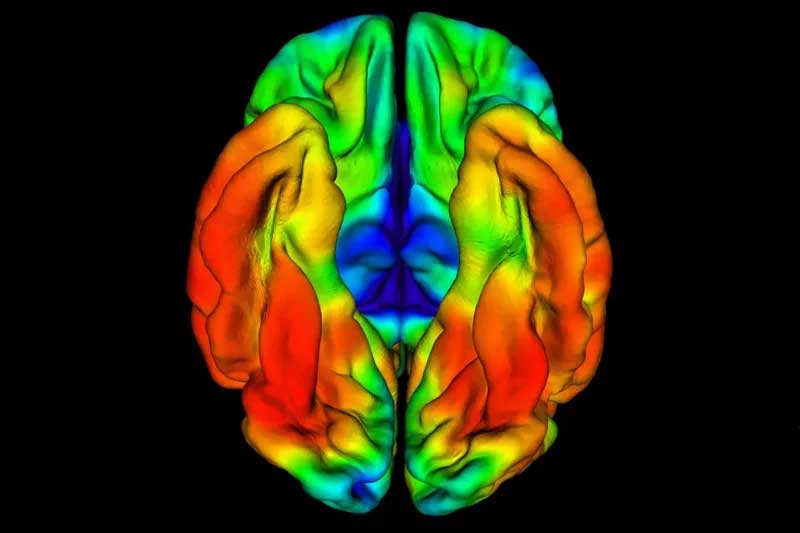
Dieser PET-Scan zeigt das Gehirn eines kolumbianischen Mannes, dessen Gedächtnis und Denken Ende der 60er Jahre intakt blieben, obwohl er Träger einer seltenen Genvariante war, die bei Menschen in den Vierzigern fast immer die Alzheimer-Krankheit verursacht. Yakil T. Quiros-Gaviria und Justin Sanchez/Massachusetts General Hospital
Er trug eine seltene Variante des Gens, das das Protein Reelin produziert. Eine Studie an Mäusen ergab, dass diese Variante die Fähigkeit des Proteins steigerte, Tau-Verwicklungen zu reduzieren.
Obwohl sich die Studie auf eine Person konzentrierte, sorgte sie in der Welt der Hirnforschung für Aufsehen und erregte sogar die Aufmerksamkeit des amtierenden Direktors der National Institutes of Health Lawrence Tabak.
„Manchmal kann die sorgfältige Untersuchung selbst einer wirklich bemerkenswerten Person zu aufregenden Entdeckungen mit weitreichenden Konsequenzen führen“, schrieb Tabak in seinem Blog über die Entdeckung.
Nachdem die Studie des Kolumbianers veröffentlicht worden war, „begannen viele Forscher Interesse an Reelin zu zeigen“, sagte Tsai.
Allerdings hatte Tsais Team bereits die Rolle dieses Proteins bei der Entstehung der Alzheimer-Krankheit untersucht.
Im September 2023 veröffentlichte das Team eine Analyse der Gehirne von 427 Menschen. Er fand heraus, dass diejenigen, die mit zunehmendem Alter eine höhere kognitive Funktion beibehielten, tendenziell mehr Neuronen hatten, die Reelin produzieren. Im Juli 2024 veröffentlichte das Team in der Fachzeitschrift Nature eine Studie, die weitere Beweise zur Stützung von Reelins Hypothese lieferte.
Die Studie umfasste eine sehr detaillierte Post-Mortem-Analyse der Gehirne von 48 Personen. Es wurden 26 Organe von Menschen entnommen, die Symptome der Alzheimer-Krankheit zeigten. Der Rest stammte von Menschen, die zum Zeitpunkt des Todes offenbar über normales Denken und Gedächtnis verfügten.
Interessanterweise hatten einige dieser scheinbar gesunden Menschen ein Gehirn voller Amyloid-Plaques.
„Wir wollten herausfinden, was das Besondere an diesen Menschen ist?“ sagt Tsai.
Deshalb analysierte das Team Neuronen in sechs verschiedenen Gehirnregionen genetisch. Sie fanden mehrere Unterschiede, darunter einen überraschenden im entorhinalen Kortex, der gleichen Region, die beim Columbia-Menschen vor Tau-Verwicklungen geschützt zu sein schien.
„Die Neuronen im entorhinalen Kortex, die bei der Alzheimer-Krankheit am anfälligsten für Neurodegeneration sind, haben eines gemeinsam“, sagt Tsai: „Sie exprimieren Reelin stark.“
Mit anderen Worten: Die Alzheimer-Krankheit scheint selektiv Neuronen zu schädigen, die Reelin produzieren, ein Protein, das für den Schutz des Gehirns vor Krankheiten unerlässlich ist. Dadurch sinkt der Reelin-Spiegel und das Gehirn wird anfälliger.
Die Entdeckung steht im Einklang mit dem, was Wissenschaftler von einem kolumbianischen Mann gelernt haben, dessen Gehirn der Alzheimer-Krankheit trotzte. Er trug eine Variante des RELN-Gens, die das Protein anscheinend wirksamer machte. Dadurch könnte ein eventuell durch die Alzheimer-Krankheit verursachter Reelin-Mangel ausgeglichen werden.
Arboleda-Velazquez sagte, die Studie bestätige zumindest „die Bedeutung von Reelin, die meiner Meinung nach übersehen wurde.“
Ohne die Zusammenarbeit von etwa 1.500 Mitgliedern einer großen kolumbianischen Familie, die Träger der Paisa-Genvariante sind, wäre Reelins Geschichte möglicherweise nie passiert.
Die ersten Mitglieder dieser Familie wurden in den 1980er Jahren von Dr. Francisco Lopera Restrepo, Leiter der Abteilung für klinische Neurologie an der Universität von Antioquia, identifiziert. Seitdem haben Familienmitglieder an einer Reihe von Studien teilgenommen, darunter an Versuchen zu experimentellen Medikamenten gegen die Alzheimer-Krankheit.
Während dieser Zeit identifizierten Wissenschaftler mehrere Familienmitglieder, die die Paisa-Genvariante erbten, aber ihre kognitive Gesundheit weit über das Alter hinaus beibehielten, in dem sich typischerweise Demenz entwickelt.
Einige scheinen durch eine äußerst seltene Version des APOE-Gens namens Christchurch-Variante geschützt zu sein, während andere durch das für Reelin verantwortliche Gen geschützt zu sein scheinen.
Beide Entdeckungen wurden möglich, weil einige Mitglieder der kolumbianischen Familie in ihrem Heimatland wiederholten Untersuchungen unterzogen wurden und sogar für Gehirnscans und andere komplexe Tests nach Boston flogen.
„Diese Menschen stimmten zu, an der Studie teilzunehmen, Blut zu spenden und ihr Gehirn nach dem Tod zu spenden“, sagt Arboleda-Velázquez. „Und sie haben die Welt verändert.“
Dopamin beschleunigt die „Reinigung“ des Gehirns bei Patienten mit Alzheimer-Krankheit, was den Gedächtnisverlust deutlich verlangsamt. Japanische und europäische Neurowissenschaftler haben herausgefunden, dass die Einführung großer Mengen Dopamin in die Gehirne von Mäusen, die für die Entwicklung der Alzheimer-Krankheit prädisponiert sind, zu einer beschleunigten Produktion des Enzyms führt, das für die Zerstörung pathogener Beta-Amyloid-Proteinmoleküle verantwortlich ist. Dadurch wird der Gedächtnisverlust deutlich verlangsamt, berichtete der Pressedienst des japanischen RIKEN Brain Research Center.
„Wir haben gezeigt, dass die Dopamin-Vorläufertherapie die Konzentration gefährlicher Beta-Amyloid-Ansammlungen reduziert und das Gedächtnis von Mäusen verbessert, die anfällig für die Entwicklung der Alzheimer-Krankheit sind. „Die Untersuchung der Mechanismen, wie Dopamin die Produktion des Neprilysin-Enzyms reguliert, wird dazu beitragen, neue Therapien zu entwickeln, um die Entwicklung der Alzheimer-Krankheit zu verhindern“, sagte Naoto Watamura, Forscher am RIKEN Brain Research Center, wie vom Pressedienst der Organisation zitiert.
Die Forscher machten diese Entdeckung, als sie die intrazellulären Mechanismen untersuchten, die die Produktion des Enzyms Neprilysin im Gehirngewebe von Säugetieren beeinflussen. Dieses Protein zerstört Beta-Amyloid-Moleküle und anderen Proteinmüll in den Neuronen gesunder Menschen und Tiere, weshalb Störungen in seiner Produktion zur Entstehung der Alzheimer-Krankheit und anderer Demenzformen beitragen.
Japanische und europäische Biologen interessierten sich dafür, ob Neuronen dazu gebracht werden könnten, Neprilysin aktiver zu produzieren, indem man eines der bereits vorhandenen Hormone oder Signalmoleküle in den Körper einführt. So schufen Wissenschaftler eine spezielle Kultur von Neuronen in der Hirnrinde, im Hippocampus und in tiefen Teilen des Gehirns von Mäusen und überwachten, wie sich die Zugabe verschiedener Substanzen auf die Aktivität des NEP-Gens auswirkte, das für die Produktion von Neprilysin verantwortlich ist.
Diese Experimente zeigten, dass die Verabreichung des Lusthormons Dopamin oder seines Vorläufers, des L-DOPA-Moleküls, die Aktivität des NEP-Gens deutlich steigerte und zu einem Anstieg der Neprilysin-Konzentration und zur Clearance von Beta-Amyloid aus Neuronen führte. Die Entdeckung zwang Wissenschaftler dazu, herauszufinden, wie sich die Einführung von L-DOPA in den Körper von Mäusen, die für die Entwicklung der Alzheimer-Krankheit prädisponiert sind, sowie die erzwungene Aktivierung von Dopamin-Neuronen auf deren Gehirnfunktion auswirken würden.
Experimente zeigten, dass die Konzentration von Beta-Amyloid in den Neuronen des Mäusekortex innerhalb weniger Wochen nach Beginn der Therapie merklich abnahm, wodurch sich die Mäuse deutlich häufiger und besser an Informationen über potenzielle Gefahren in ihren Gehegen erinnerten. L-DOPA-basierte Medikamente werden bereits zur Behandlung der Parkinson-Krankheit eingesetzt, was Hoffnung auf die rasche Entwicklung von Ansätzen gibt, die die Clearance von Beta-Amyloid aus den Gehirnen von Alzheimer-Trägern beschleunigen, so die Schlussfolgerung der Wissenschaftler.
Die Alzheimer-Krankheit ist eine der häufigsten Formen der Altersdemenz. Laut Wissenschaftlern entsteht es durch die Ansammlung von Beta-Amyloid in Neuronen – toxische Proteinknäuel, die aus beschädigten APP-Proteinmolekülen bestehen. Neben Beta-Amyloid reichern sich während der Entwicklung der Alzheimer-Krankheit auch andere toxische Moleküle in Gehirnzellen an, darunter beschädigte Tau-Proteinstränge.