Wissenschaftler haben Zehntausende mysteriöser „Knoten“ in der menschlichen DNA identifiziert, die möglicherweise eine Schlüsselrolle bei der Steuerung der Genaktivität spielen. Die Aktivität von 4-strängiger DNA in lebenden Zellen wurde enthüllt. Synthetische DNA wurde mit vier zusätzlichen Buchstaben erstellt. DNA verdreht sich in seltsame Formen, um sich in Zellen einzufügen.
Wissenschaftler haben Zehntausende mysteriöser „Knoten“ in der menschlichen DNA identifiziert, die möglicherweise eine Schlüsselrolle bei der Steuerung der Genaktivität spielen. Die Kenntnis der genauen Lage dieser Knoten, sogenannte „i-Motive“, könnte nach Ansicht der Forscher, die hinter der Arbeit stehen, zur Entwicklung neuer Behandlungsmethoden für Krankheiten, einschließlich Krebs, führen.
DNA besteht aus Bausteinen, sogenannten Nukleotiden, von denen jeder eine der folgenden Basen trägt: Adenin, Guanin, Thymin oder Cytosin. Diese Basen sind die einzelnen Buchstaben, aus denen der DNA-Code besteht. DNA hat eine Leiterstruktur und typischerweise paaren sich die Basen auf einer Seite der Leiter mit einem Partner auf der anderen Seite, die sich in der Mitte verbinden, um die Sprossen der Leiter zu bilden. Adenin paart sich mit Thymin und Guanin paart sich mit Cytosin.
Manchmal können sich Cytosine jedoch eher miteinander als mit Guanin paaren. Dadurch dreht sich das DNA-Molekül um sich selbst und es entsteht eine viersträngige, hervorstehende Struktur, die als i-Motiv bezeichnet wird.
Forscher entdeckten erstmals 2018 i-Motive in menschlichen Zellen. Damals vermuteten sie, dass diese Knoten wichtige Regulatoren des Genoms sein könnten und dabei helfen könnten, zu steuern, welche Gene ein- oder ausgeschaltet werden. Allerdings wusste man bisher wenig darüber, wo genau sich diese knorrigen Strukturen befinden und wie viele es im menschlichen Genom gibt.
In einer neuen Studie, die am 29. August im EMBO Journal veröffentlicht wurde, kartierten Forscher 50.000 i-Motive. Diese i-Motive befinden sich im gesamten Genom, kommen jedoch typischerweise in DNA-Regionen vor, die die Genaktivität steuern, stellten die Autoren der Studie fest.
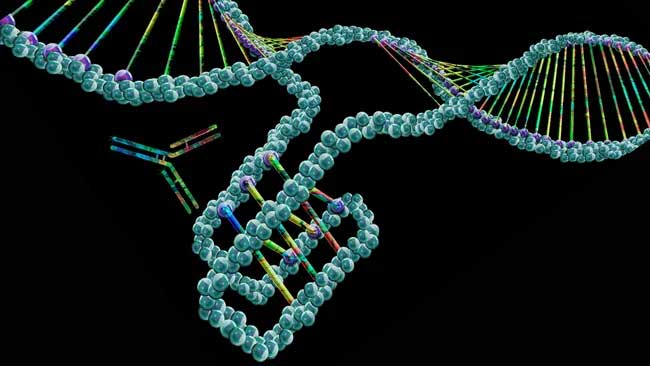
In der neuen Studie kartierten Wissenschaftler 50.000 knotenartige Strukturen in der DNA, die als „i-Motive“ bekannt sind. KEITH CHAMBERS/WISSENSCHAFTLICHE FOTOBIBLIOTHEK
„Unsere Ergebnisse bestätigen, dass i-Motive nicht nur eine Laborkuriosität sind, sondern ein weit verbreitetes Phänomen, das wahrscheinlich eine Schlüsselrolle bei der Genomfunktion spielt“, sagte Daniel Christ, Co-Autor der Studie und Direktor des Zentrums für gezielte Therapien des Instituts, in einer Erklärung . Garvan Medical Research in Australien.
Christ und Kollegen entdeckten i-Motive in DNA, die im Labor aus menschlichen Zellen extrahiert wurde. Sie identifizierten diese Knoten mithilfe von Antikörpern, die die i-Motive spezifisch erkennen und mit ihnen komplexieren sollen. Anschließend reinigte das Team diese Antikörper-Knoten-Komplexe, um die darin enthaltene DNA zu sequenzieren.
„Wir haben herausgefunden, dass i-Motive mit Genen verbunden sind, die in bestimmten Phasen des Zellzyklus hochaktiv sind“, sagte Cristian David Peña Martinez, Hauptautor der Studie und Postdoktorand bei Garvan, in einer Erklärung. Der Zellzyklus ist der Prozess, durch den sich Zellen im Körper vermehren.
„Dies deutet darauf hin, dass sie eine dynamische Rolle bei der Regulierung der Genaktivität spielen“, fügte Pena Martinez hinzu.
Das Team entdeckte außerdem i-Motive in den „Promotor“-Regionen verschiedener krebsrelevanter Gene. Promotoren sind eine Art genetisches Material, das ein bestimmtes Gen wie einen Lichtschalter ein- und ausschaltet. In Krebszellen können diese Gene fehlreguliert werden, was zu einer erhöhten Zellteilung und einem für Tumoren charakteristischen Wachstum führt.
Diese neue Entdeckung deutet darauf hin, dass i-Motive eines Tages Ziele für Krebsmedikamente werden könnten, schlug das Team vor. Sie entdeckten i-Motive in der MYC-Genfamilie, von der bekannt ist, dass sie bei etwa 70 % aller Krebserkrankungen beim Menschen gestört ist.
„Dies stellt eine aufregende Gelegenheit dar, krankheitsassoziierte Gene durch die i-Motiv-Struktur anzusprechen“, sagte Pena Martinez. Natürlich ist noch mehr Forschung nötig, um diese Idee von der Theorie in die Praxis bei Krebspatienten umzusetzen.
Die Aktivität von 4-strängiger DNA in lebenden Zellen wurde enthüllt. Zwei dünne Stränge, die zu einer Spirale zusammengedreht sind, sind die ikonische Form des DNA-Moleküls. Aber manchmal kann DNA eine seltene Vierfachhelix bilden, und diese seltsame Struktur könnte bei Krankheiten wie Krebs eine Rolle spielen.
Über diese viersträngigen DNAs, die als G-Quadruplexe bekannt sind, ist nicht viel bekannt, aber Wissenschaftler haben jetzt eine neue Methode entwickelt, um diese seltsamen Moleküle zu erkennen und zu beobachten, wie sie sich in lebenden Zellen verhalten. In einer am 8. Januar 2021 in der Fachzeitschrift Nature Communications veröffentlichten Studie beschrieb das Team, wie bestimmte Proteine die Auflösung des G-Quadruplex bewirken; Ihre Arbeit könnte in Zukunft zu neuen Medikamenten führen, die viersträngige DNA einfangen und deren Aktivität stören. Medikamente können zum Beispiel eingreifen, wenn fremde DNA das Wachstum eines Krebstumors fördert.
„Es gibt immer mehr Hinweise darauf, dass G-Quadruplexe eine wichtige Rolle bei einer Vielzahl lebenswichtiger Prozesse sowie bei einer Reihe von Krankheiten spielen“, sagte Studienautor Ben Lewis vom Department of Chemistry am Imperial College London in einer Erklärung .
Generell kommen G-Quadruplexe in Krebszellen deutlich häufiger vor als in gesunden Zellen, heißt es in der Stellungnahme. Verschiedene Studien haben das Vorhandensein von viersträngiger DNA mit der schnellen Teilung von Krebszellen in Verbindung gebracht, einem Prozess, der zum Tumorwachstum führt; Daher stellten Wissenschaftler die Hypothese auf, dass Medikamente, die auf die seltsame DNA abzielen, diese ungezügelte Zellteilung verlangsamen oder stoppen könnten. Einige Studien unterstützen diese Idee bereits.
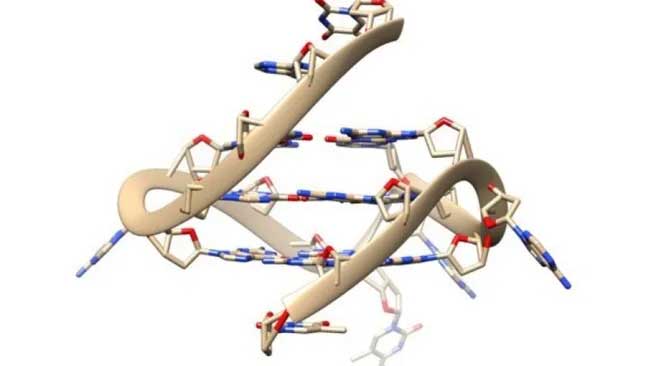
G-Quadruplexe. Imperial College London
„Aber das fehlende Glied bestand darin, diese Struktur direkt in lebenden Zellen abzubilden“, sagte Lewis. Mit anderen Worten: Wissenschaftler brauchten eine bessere Möglichkeit, diese DNA-Moleküle in Aktion zu beobachten. Neue Forschung beginnt, dieses fehlende Wissen zu ergänzen.
Laut Discover Magazine können sich G-Quadruplexe entweder bilden, wenn sich ein einzelnes doppelsträngiges DNA-Molekül in sich selbst faltet, oder wenn mehrere DNA-Stränge zu einer einzigen Nukleinsäure, bekannt als Guanin, einem der Bausteine der DNA, zusammengefügt werden. Um diese ungewöhnliche DNA in Zellen nachzuweisen, verwendete das Team eine Chemikalie namens DAOTA-M2, die fluoreszierendes Licht aussendet, wenn sie an G-Quadruplexe bindet. Anstatt einfach die Helligkeit des Lichts zu messen, die sich je nach Konzentration der DNA-Moleküle ändert, verfolgte das Team auch, wie lange das Licht eingeschaltet war.
Durch die Verfolgung der Verweildauer des Lichts konnte das Team erkennen, wie verschiedene Moleküle mit viersträngiger DNA in lebenden Zellen interagieren. Als sich das Molekül an einen DNA-Strang anheftete, löste es das leuchtende DAOTA-M2, wodurch das Licht schneller verblasste, als wenn die Chemikalie an Ort und Stelle geblieben wäre. Mit diesen Methoden identifizierte das Team zwei Proteine, sogenannte Helikasen, die Stränge viersträngiger DNA abwickeln und den Prozess ihres Abbaus auslösen.
Sie identifizierten auch andere Moleküle, die an DNA binden; Zukünftige Studien zu diesen molekularen Wechselwirkungen könnten Wissenschaftlern dabei helfen, Medikamente zu entwickeln, die an DNA binden.
„Viele Forscher haben sich für das Potenzial von G-Quadruplex-Bindungsmolekülen als potenzielle Medikamente gegen Krankheiten wie Krebs interessiert“, sagte Ramon Vilar, Professor für medizinische anorganische Chemie am Imperial, in einer Erklärung. „Unsere Methode wird uns helfen, unser Verständnis dieser potenziellen neuen Medikamente zu verbessern.“
Die Forscher erstellten synthetische DNA unter Verwendung von vier zusätzlichen Molekülen, sodass das resultierende Produkt einen Code aus acht statt vier Buchstaben hatte. Mit der Zunahme der Buchstabenzahl erlangte diese DNA eine viel größere Kapazität zur Speicherung von Informationen. Die Wissenschaftler nannten die neue DNA „Hachimoji“ – was auf Japanisch „acht Buchstaben“ bedeutet – und erweiterten damit frühere Arbeiten verschiedener Gruppen, die ähnliche DNA aus sechs Buchstaben erstellten.
Eine am 20. Februar 2019 in der Fachzeitschrift „Science“ veröffentlichte Studie bestätigt die letztgenannte Annahme: Wissenschaftler haben kürzlich einen neuen DNA-Typ mit einer eleganten Doppelhelix-Struktur gebildet und herausgefunden, dass dieser über Eigenschaften verfügt, die das Leben unterstützen könnten.
Natürliche DNA besteht aus vier Molekülen, den sogenannten Stickstoffbasen, die miteinander verbunden sind und den Code für das Leben auf der Erde bilden: A bindet an T; G bindet an C. Hachimoji-DNA umfasst diese vier natürlichen Basen sowie vier weitere synthetische Nukleotidbasen: P, B, Z und S.
Das Forschungsteam, dem mehrere verschiedene Teams in den Vereinigten Staaten angehörten, schuf Hunderte dieser Hachimoji-Doppelhelices mit unterschiedlichen Kombinationen natürlicher und synthetischer Nukleotidbasenpaare. Anschließend führten sie eine Reihe von Experimenten durch, um herauszufinden, ob verschiedene Doppelhelices über die notwendigen Eigenschaften verfügen, um Leben zu ermöglichen.
Natürliche DNA hat eine besondere Eigenschaft, die kein anderes genetisches Molekül zu haben scheint: Sie ist stabil und vorhersehbar. Dies bedeutet, dass Forscher genau berechnen können, wie es sich bei bestimmten Temperaturen und Umgebungen verhält und wann es zu zerfallen beginnt.
Aber es stellte sich heraus, dass die Forscher dasselbe mit Hachimojis DNA tun konnten – sie konnten eine Reihe von Regeln entwickeln, die die Stabilität der DNA vorhersagen konnten, wenn sie unterschiedlichen Temperaturen ausgesetzt wurde.
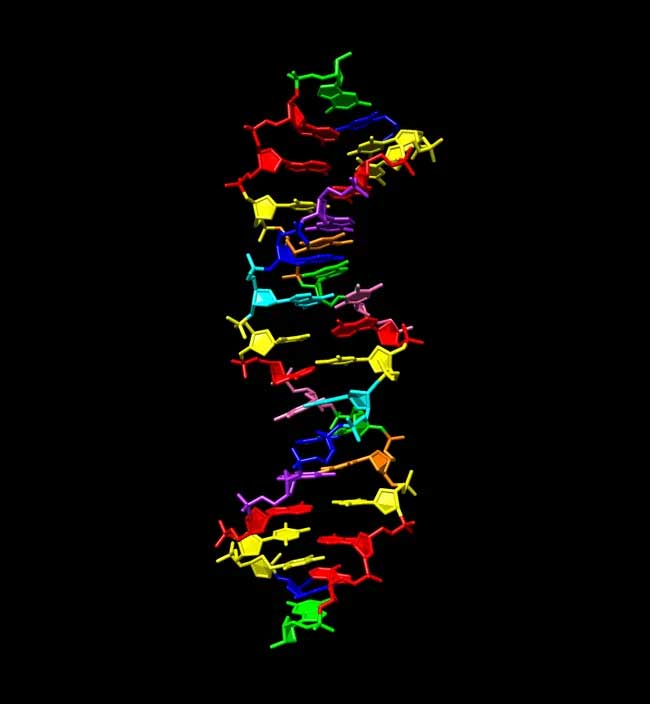
Forscher haben im Labor einen neuen DNA-Typ entwickelt, der aus acht statt der natürlichen vier Buchstaben besteht. Millie Georgiadis, Medizinische Fakultät der Indiana University
Aber es reicht nicht aus, DNA zu schaffen, die Informationen speichert. Es muss diese Informationen auch an sein Schwestermolekül, die RNA, weitergeben können, damit diese RNA dann Proteine anweisen kann, alle Dinge im Körper zu tun.
Vor diesem Hintergrund entwickelten die Forscher synthetische Enzyme – Proteine, die die Reaktion erleichtern –, die Hachimoji-DNA erfolgreich in Hachimoji-RNA kopierten. Darüber hinaus entdeckten sie, dass sich das RNA-Molekül in eine Art L-Form falten kann, was für die weitere Informationsübertragung notwendig ist.
Darüber hinaus müssen sich die DNA-Stränge zu derselben dreidimensionalen Struktur – der berühmten Doppelhelix – verdrehen können.
Das Team erstellte drei Kristallstrukturen von Hachimojis DNA, jede mit einer anderen Sequenz von acht Basenpaaren, und stellte fest, dass jede tatsächlich eine klassische Doppelhelix bildete.
Damit Hachimojis DNA jedoch das Leben unterstützt, gibt es eine fünfte Voraussetzung, sagte Benner. Das heißt, es muss sich selbst tragen oder aus eigener Kraft überleben können. Allerdings untersuchten die Forscher diesen Schritt nicht, um zu verhindern, dass das Molekül zu einer biologischen Gefahr wird, die sich eines Tages in die Genomen von Organismen auf der Erde einschleichen könnte.
Dieser aus acht Buchstaben bestehende DNA-Strang bietet nicht nur Einblicke in Alternativen zum Leben im Weltraum, sondern hat auch Anwendungen auf unserem Planeten. Das aus acht Buchstaben bestehende genetische Alphabet würde mehr Informationen speichern und sich spezifischer an bestimmte Ziele binden, sagte Benner. Hachimoji-DNA könnte beispielsweise zur Bindung an Leberkrebszellen oder Anthrax-Toxine oder zur Beschleunigung chemischer Reaktionen verwendet werden.
„Wenn die Anzahl der Buchstaben von sechs auf acht steigt, nimmt die Vielfalt der DNA-Sequenzen deutlich zu“, schrieb Ichiro Hirao, ein synthetischer Molekularbiologe am A*STAR Institute of Bioengineering and Nanotechnology in Singapur, der ebenfalls nicht an der Studie beteiligt war eine E-Mail. (Hiraos Gruppe war jedoch auch an einer früheren Studie beteiligt, bei der DNA-Stränge mit sechs Buchstaben erstellt wurden.)
Natürlich „ist dies nur die erste Demonstration“ der aus acht Buchstaben bestehenden Doppelhelix der DNA, und für den praktischen Einsatz müssen wir die Genauigkeit und Effizienz der Replikation und Transkription in RNA verbessern, sagte Hirao in einer E-Mail. Er schlägt vor, dass sie die Anzahl der Buchstaben irgendwann auf noch mehr erweitern können.
Im Jahr 2021 nahmen Wissenschaftler hochauflösende Videos auf, die zeigen, wie DNA seltsame Formen annimmt, um sich in Zellen hineinzuquetschen.
Im Jahr 1952 machte Rosalind Franklin das erste indirekte Foto der DNA, indem sie untersuchte, wie Röntgenstrahlen von diesen Grundmolekülen reflektiert werden. Doch erst 2012 machten Wissenschaftler mit einem Elektronenmikroskop ein direktes Foto der DNA. Jetzt hat ein Forscherteam im Vereinigten Königreich mithilfe einer Kombination aus fortschrittlicher Mikroskopie und Modellierung hochauflösende Videos von DNA in Bewegung aufgenommen.
Menschliche Zellen enthalten etwa 2 Meter DNA. Angesichts der Tatsache, dass menschliche Zellen in der Größenordnung von Mikrometern liegen, muss die DNA wirklich gut darin sein, sich zu „supercoiling“, also zu biegen und zu falten, um sich fest in der Zelle zu verdichten. Doch bis vor Kurzem war die Technologie nicht gut genug, um Wissenschaftlern klar zu zeigen, wie die Struktur der DNA in einem supergewundenen Zustand aussieht, schreiben die Autoren in der Studie.
Um diese Frage zu beantworten, griffen die Autoren der neuen Studie auf „Mini-DNA-Kreise“ zurück, die aus Bakterien isoliert und hergestellt wurden. Diese zirkulären DNA-Strukturen kommen auch in menschlichen Zellen vor und ihre Funktion ist weitgehend unbekannt. Die Forscher verwendeten diese Ringstrukturen, weil Wissenschaftler sie auf eine Weise verdrehen können, die mit langen Strängen, der häufigsten Form der DNA, nicht funktionieren würde, heißt es in der Erklärung.
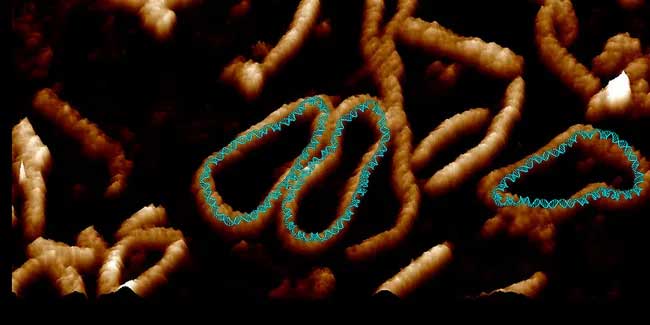
DNA. Universität Leeds
Um die Bewegungen im Detail zu untersuchen, verwendeten die Forscher eine Kombination aus Supercomputersimulationen und Rasterkraftmikroskopie, bei der eine scharfe Spitze über die Oberfläche eines Moleküls gleitet und die Kräfte misst, die die Spitze abstoßen, um die Struktur abzubilden.
„Sehen ist Glauben, aber bei einem so kleinen Objekt wie DNA war es äußerst schwierig, die helikale Struktur des gesamten DNA-Moleküls zu erkennen“, sagte Studienleiterin Alice Pyne, Dozentin für Polymere und weiche Materie an der University of Sheffield im Vereinigten Königreich. Wer hat die neuen Daten aufgezeichnet, sagte Frames in einer Erklärung. „Die von uns entwickelten Videos ermöglichen es uns, die Verdrehung der DNA in einem noch nie dagewesenen Detaillierungsgrad zu beobachten.“
Die Mikroskopbilder waren so detailliert, dass sie die Doppelhelixstruktur der DNA erkennen konnten. Nachdem die Forscher diese Bilder mit Simulationen kombiniert hatten, konnten sie laut Aussage die Position jedes einzelnen Atoms in der DNA sehen, während es sich bewegte.
Interessanterweise bewegte sich die DNA in ihrer entspannten Form kaum. Aber wenn die DNA verdreht wurde – wie es normalerweise der Fall ist, wenn sie in eine Zelle gepresst wird –, verwandelte sie sich in viele andere Formen, heißt es in der Aussage. Diese unterschiedlichen Formen beeinflussten die Interaktion und Bindung des DNA-Moleküls mit anderen DNA-Molekülen um es herum, schreiben die Autoren in der Arbeit.
Lynn Zechidrich, Professorin am Baylor College of Medicine in Houston, Texas, die die Miniringe für die Studie zur Verfügung stellte, hatte zuvor herausgefunden, wie man diese Ringstrukturen als Vektoren für die Gentherapie nutzen kann, indem man kleine genetische Botschaften in die Ringe einfügt.
Wissenschaftler, die die Studie durchgeführt haben, „haben eine Technik entwickelt, die sehr detailliert zeigt, wie faltig, sprudelnd, gebogen, denaturiert und seltsam geformt sie sind“, sagte Zechidrich, der nicht direkt an der Studie beteiligt war, in einer Erklärung. „Wir müssen verstehen, wie sich Supercoiling, das für die DNA-Aktivität in Zellen so wichtig ist, auf die DNA auswirkt, in der Hoffnung, dass wir eines Tages lernen, es nachzuahmen oder zu kontrollieren.“