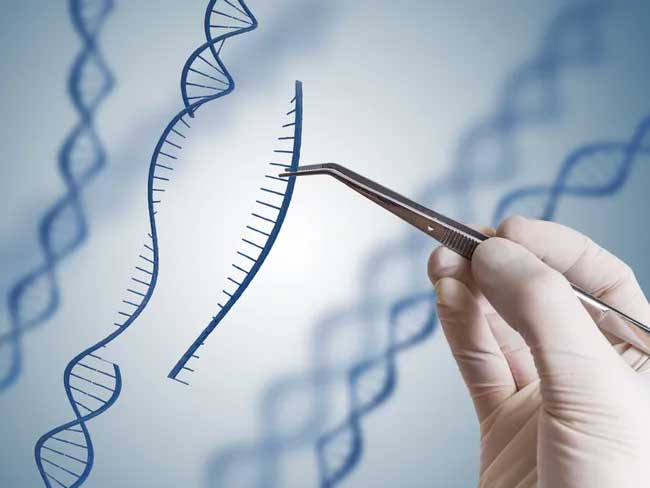
Die MHRA hat Casgevy für die Behandlung der Sichelzellenanämie (SCD) und der transfusionsabhängigen Beta-Thalassämie zugelassen. Hierbei handelt es sich um lebenslange genetische Störungen, die durch Mutationen in den Genen verursacht werden, die für Hämoglobin kodieren, ein Protein, das die roten Blutkörperchen für den Sauerstofftransport durch den Körper benötigen. CRISPR könnte eine häufige Form der erblichen Blindheit behandeln. Der Nobelpreis für Chemie 2020 ging an zwei Frauen, die ein Gen-Editing-Tool namens CRISPR-Cas9 entwickelt haben, das DNA wie eine molekulare Schere schneidet.
Im Sommer 2012 stellten Wissenschaftler der Welt CRISPR als Werkzeug zur Genbearbeitung vor, als wegweisende Arbeiten von zwei unabhängigen Gruppen zeigten, wie das System zum Schneiden von DNA eingesetzt werden kann. Wir sehen jetzt, dass CRISPR in innovativen medizinischen Behandlungen eingesetzt wird.
Vor diesen bahnbrechenden Arbeiten begannen andere Forscher zu entschlüsseln, wie CRISPR im Inneren von Mikroben funktioniert. Obwohl CRISPR vor allem als Werkzeug zur Genbearbeitung bekannt ist, wurde es erstmals in Bakterien entdeckt und Wissenschaftler erkannten, dass es als eine Art Immunsystem fungiert – eine Abwehr gegen Viren. In diesem Immunsystem verfügt das Bakterium über eine Speicherbank voller genetischem Material des Virus. Das Bakterium wird dieses Material behalten, nachdem es vom Virus angegriffen wurde, um sich vor künftigen Invasionen zu schützen.
Diese Speicherbank ist mit winzigen molekularen Scheren namens Cas-Proteinen gepaart, die DNA schneiden, und einem Molekül, das die Schere zu ihrem Ziel führt. Bei Bakterien ist dieses Ziel ein viraler Eindringling. Šikšnis und seine Kollegen zeigten, dass Wissenschaftler diese Schere zu ihrem Vorteil nutzen und auf jede DNA zielen können, die sie bearbeiten möchten. Dies demonstrierten sie konkret am Beispiel des Cas9-Proteins.
Zusammen mit Jennifer Doudna und Emmanuelle Charpentier – Autoren eines weiteren bahnbrechenden Artikels über CRISPR, der 2012 veröffentlicht wurde – wurde Sikshnis für seine Erfindung von CRISPR-Cas9, einem „Präzisions-Nanotool für die DNA-Bearbeitung“, mit dem Kavli-Preis für Nanowissenschaften 2018 ausgezeichnet. Er und sein Team erforschen derzeit die Vielfalt der in der Natur vorkommenden CRISPR-Systeme, um herauszufinden, welche für die Gestaltung von Genomen nützlich sein könnten.
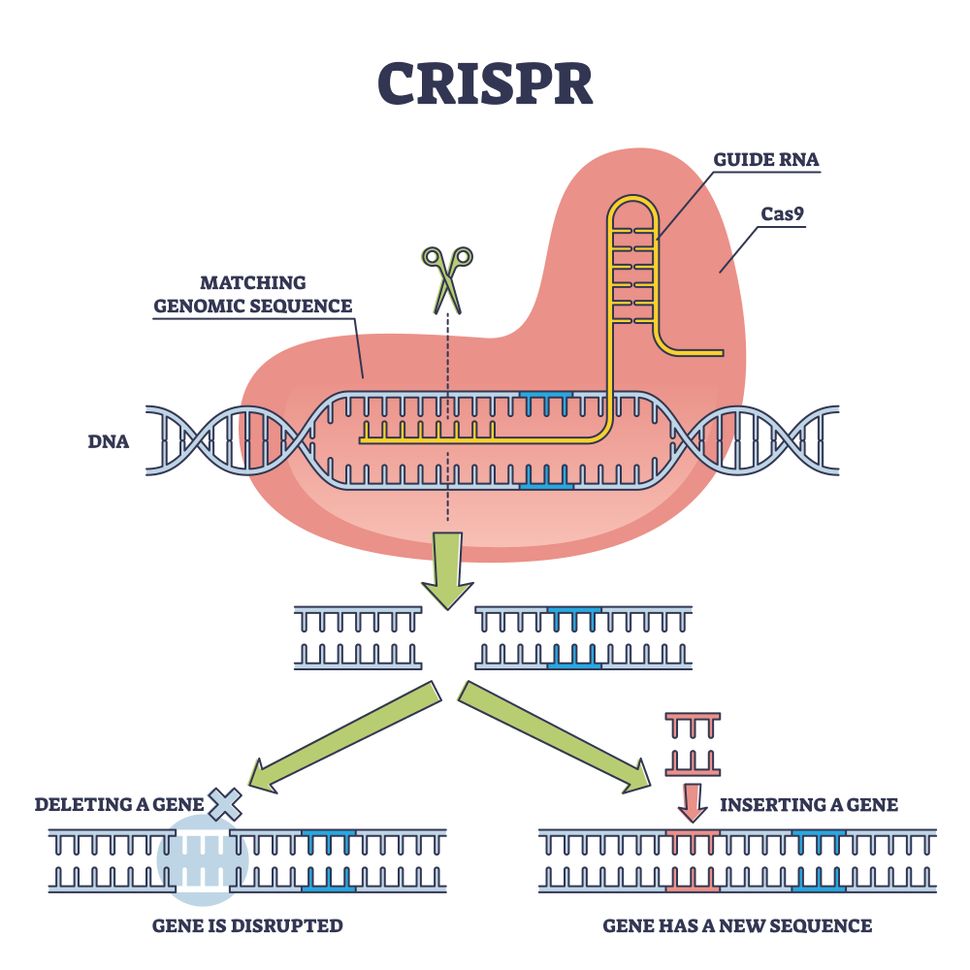
Das CRISPR-Cas9-System nutzt Cas9 als molekulare Schere und ein RNA-Molekül als Führung für die Schere.
Eine Arbeit aus dem Jahr 2012 zeigte, dass es möglich ist, das Cas9-Protein umzuprogrammieren und es auf jede beliebige Sequenz im Genom auszurichten. Es ist wirklich ein wirklich vielseitiges System, das für die Genombearbeitung in einer Vielzahl von Modellorganismen verwendet werden kann.
Diese Behandlung weist mehrere Einschränkungen auf, da in diesem Fall die Behandlung ex vivo erfolgt. Das bedeutet, dass die zu behandelnden Zellen aus dem Körper des Patienten entfernt werden und dann ein Cas9-Werkzeug verwendet wird, um die Mutation zu korrigieren – oder im Wesentlichen die Produktion von fötalem Hämoglobin auszulösen. Und dann müssen diese manipulierten Zellen wieder in den Körper des Patienten zurückgeführt werden. Und natürlich handelt es sich hierbei um eine Art komplexes und langwieriges Verfahren.
Natürlich wäre es großartig, wenn CRISPR-Behandlungen direkt im menschlichen Körper durchgeführt werden könnten – wir nennen das in vivo. Um dies zu erreichen, müssen jedoch in Wirklichkeit mehrere Herausforderungen bewältigt werden: Erstens müssen wir dieses CRISPR-Tool in bestimmte Gewebe oder Organe des menschlichen Körpers bringen. Und natürlich gibt es viele Möglichkeiten, CRISPR-Tools bereitzustellen, aber seit COVID sind mRNA-Impfstoffe als therapeutische Option zur Behandlung und Prävention von COVID zugelassen. Und mittlerweile ist mRNA in Kombination mit Lipid-Nanopartikeln zu einer der Schlüsselmethoden geworden, um Cas9 in verschiedene Zellen und Gewebe des menschlichen Körpers zu transportieren.
Es werden auch andere Transportsysteme erforscht, darunter virusähnliche Partikel und Adeno-assoziierte Viren. Daher werden AAVs auch als Transportmittel verwendet und sind als sichere Transportmittel in den menschlichen Körper zugelassen. Allerdings gibt es bei AAVs beispielsweise eine Beschränkung der Verpackungslast und man muss kleinere Werkzeuge zur Genbearbeitung finden, die in einem verpackt werden können AAV-Partikel.

Virginijus Siksnis untersucht die Vielfalt der in der Natur vorkommenden CRISPR-Systeme. Universität Vilnius
Zunächst untersuchen Forscher mikrobielle DNA-Sequenzen, die in riesigen Datenbanken vorhanden sind, in denen neue CRISPR-Systeme zu finden sind. Anschließend wird versucht, sie in verschiedenen Bakterien zu exprimieren, zu isolieren, zu charakterisieren und dann in menschliche Zellen zu übertragen, um zu prüfen, ob sie als neue Werkzeuge zur Genommodifikation verwendet werden können.
Es war von Anfang an klar, dass genetische Krankheiten, die durch eine einzelne Mutation verursacht werden, wie beispielsweise die Sichelzellenanämie, das erste Angriffsziel sein würden. Dies schien leicht zu erreichen, da nur eine Mutation im Genom korrigiert werden musste. Ein Teil des Verdienstes für diese Cas9-basierte Sichelzellenanämie-Behandlung sollte den Menschen zuteil werden, die sich seit Jahrzehnten mit der Sichelzellenanämie befassen. Sie lieferten Einblicke in Krankheitsmechanismen, die an der Behandlung beteiligt waren.
CRISPR-Cas9 ist eine Art universelle oder multifunktionale Technologie, da mit ihr jeder lebende Organismus erschaffen werden kann. Sie versuchen lediglich, DNA zu erschaffen, und DNA ist der Bauplan für jeden lebenden Organismus. Anstatt also die Genbearbeitung in menschlichen Zellen vorzunehmen, sollten Sie vielleicht auch über die Bearbeitung einer Bakterienpopulation nachdenken – beispielsweise derjenigen, die im menschlichen Darm vorkommen. Und diese Bakterienpopulationen können entstehen.
CRISPR-Technologien können auch als antivirale Wirkstoffe eingesetzt werden. Derzeit ist das Problem mit Antibiotika ziemlich klar – wir verlieren wahrscheinlich unseren Kampf gegen Bakterien durch den Einsatz von Antibiotika. Es werden immer neue Antibiotika benötigt und diese sind wirklich schwer zu finden, schwierig und teuer. Daher werden alternative Technologien entwickelt, beispielsweise die Virustherapie oder die antibakteriellen CRISPR-Systeme.
CRISPR wurde vor einigen Jahren in China zur Erzeugung menschlicher Embryonen eingesetzt – das ist also eine Grenze, die Wissenschaftler eigentlich nicht überschreiten wollen, weil sie wirklich gefährlich sein könnte.
Exa-cel, auch bekannt unter dem Markennamen Casgevy, erhielt am 16. November 2023 seine erste behördliche Zulassung von der britischen Regulierungsbehörde für Arzneimittel und Gesundheitsprodukte (MHRA) für die Behandlung von zwei schwächenden Blutkrankheiten: Sichelzellenanämie und transfusionsabhängige Betazellkrankheit. Die US-amerikanische Food and Drug Administration (FDA) genehmigte diese Therapie später zur Behandlung beider Krankheiten.
Die weltweit erste Behandlung mit der CRISPR-Genbearbeitungstechnologie wurde zugelassen. Arzneimittelbehörden haben eine CRISPR-Therapie namens Casgevy zur Behandlung erblicher Bluterkrankungen zugelassen.
Die historische Entscheidung der Aufsichtsbehörden, Casgevy zuzulassen, könnte den Beginn einer neuen Ära der Gentherapie einläuten. Es bleiben jedoch Fragen hinsichtlich der Verfügbarkeit der Behandlung und ihrer langfristigen Sicherheit.
Die MHRA hat Casgevy für die Behandlung der Sichelzellenanämie (SCD) und der transfusionsabhängigen Beta-Thalassämie zugelassen. Hierbei handelt es sich um lebenslange genetische Störungen, die durch Mutationen in den Genen verursacht werden, die für Hämoglobin kodieren, ein Protein, das die roten Blutkörperchen für den Sauerstofftransport durch den Körper benötigen.
Es wird geschätzt, dass mehr als 100.000 Menschen in den Vereinigten Staaten an SCD leiden, die Rate ist jedoch in einigen Bevölkerungsgruppen höher als in anderen. Beispielsweise wird eines von 365 schwarzen Kindern mit SCD geboren. Die Krankheit verändert die Form der roten Blutkörperchen einer Person, so dass sie C-förmig statt rund werden. Die Sichelzellen sterben schnell ab und verkleben zudem, wodurch die Blutgefäße verstopfen. Infolgedessen entwickeln die Patienten eine Anämie und erleben häufig starke Schmerzanfälle, sogenannte Schmerzkrisen.
Etwa 1 von 100.000 Menschen weltweit ist von Beta-Thalassämie betroffen, wobei Menschen aus dem Mittelmeerraum, Asien, Afrika und dem Nahen Osten überproportional betroffen sind. Patienten mit Beta-Thalassämie produzieren nicht genügend Hämoglobin, was zu schwerer Anämie führen kann, während es aufgrund eines Mangels an gesunden roten Blutkörperchen zu einer Sichelzellenanämie kommt. „Transfusionsabhängig“ bedeutet, dass die Krankheit so schwerwiegend ist, dass die Patienten ihr ganzes Leben lang regelmäßige Transfusionen roter Blutkörperchen benötigen.
Casgevy basiert auf einer revolutionären Gen-Editing-Technologie namens CRISPR, die erstmals 2012 entwickelt wurde. Das CRISPR-System schneidet mithilfe des Cas9-Enzyms Gene aus der DNA. Diese „molekulare Schere“ wird von einem RNA-Molekül auf die Ziel-DNA gerichtet. Die Technologie wurde von einem natürlichen Abwehrmechanismus übernommen, den Bakterien und andere einfache Organismen, sogenannte Archaeen, gegen Viren nutzen.
Casgevy zielt auf das BCL11A-Gen ab. Das Gen kodiert für ein Protein, das normalerweise kurz nach der Geburt den Wechsel von der fetalen Version des Hämoglobins zur adulten Version reguliert. Bei Patienten mit SCD und Beta-Thalassämie ist jedoch das adulte Hämoglobin defekt.
Das Ziel von Casgevy besteht darin, BCL11A auszuschalten und es dem Körper so zu ermöglichen, weiterhin fötales Hämoglobin zu produzieren, da die Erwachsenenversion nicht funktioniert. Dazu werden hämatopoetische Stammzellen aus dem Knochenmark des Patienten entnommen und das BCL11A-Gen im Labor mit Casgevy bearbeitet. Die veränderten Zellen mit funktionierendem Hämoglobin werden dann wieder in den Körper des Patienten infundiert. Vor der Infusion muss der Patient ein Chemotherapeutikum namens Busulfan einnehmen, um noch im Knochenmark befindliche unbearbeitete Zellen zu eliminieren, berichtet STAT News.
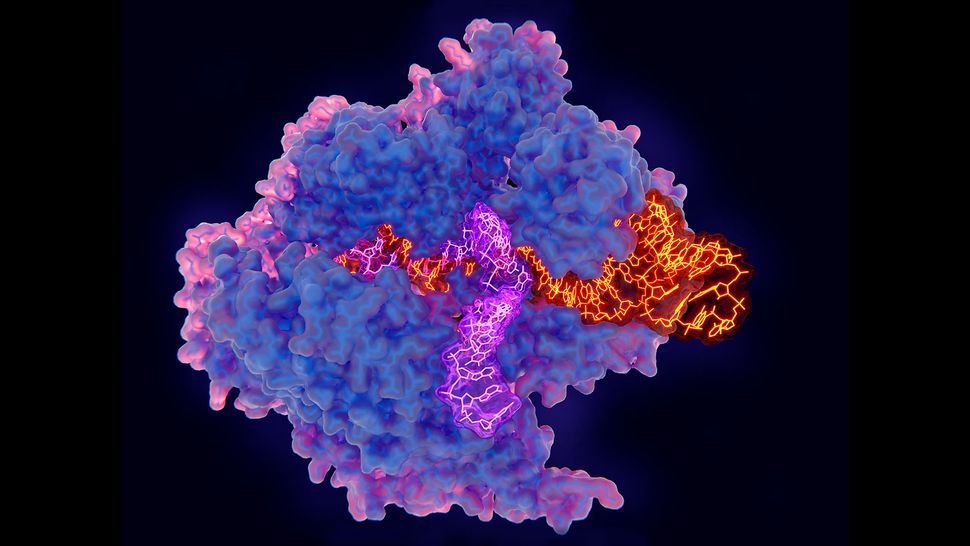
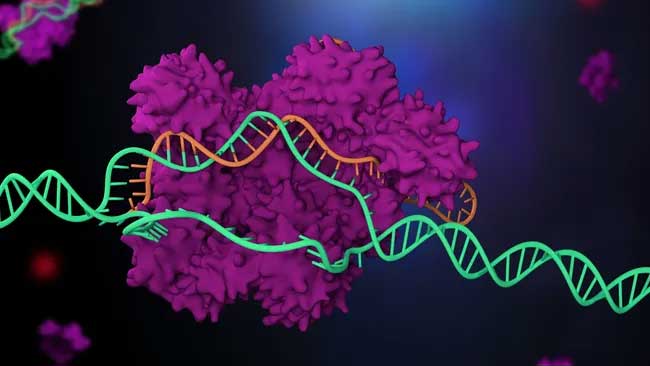
Diese Abbildung von CRISPR in Aktion zeigt Cas9 (blau und rosa), gebunden an DNA (lila), neben einem Leit-RNA-Molekül (orange). JUAN GAERTNER/WISSENSCHAFTLICHE FOTOBIBLIOTHEK
Dieser Anpassungsprozess an neue, bearbeitete Zellen ist langwierig. „Patienten müssen möglicherweise mindestens einen Monat im Krankenhaus verbringen, während sich die behandelten Zellen im Knochenmark ansiedeln und beginnen, rote Blutkörperchen mit einer stabilen Form von Hämoglobin zu produzieren“, sagte die MHRA in einer Erklärung.
In zwei klinischen Studien im Spätstadium stellte Casgevy die Hämoglobinproduktion bei den meisten Patienten mit SCD und Beta-Thalassämie wieder her und verbesserte ihre Symptome. 28 von 29 Patienten mit SCD erlebten mindestens ein Jahr nach der Behandlung mit Casgevy keine ernsthafte Schmerzkrise. Ebenso benötigten 39 von 42 Patienten mit Beta-Thalassämie im gleichen Zeitraum nach der Behandlung keine Transfusionen roter Blutkörperchen. Die übrigen drei Patienten benötigten mehr als 70 % seltener Transfusionen.
In keiner der beiden klinischen Studien mit Casgevy im Spätstadium wurden schwerwiegende Probleme bei der Arzneimittelsicherheit festgestellt, obwohl über einige vorübergehende Nebenwirkungen wie Fieber und Müdigkeit berichtet wurde. Beide Studien laufen noch und die langfristige Sicherheit von Casgevy wird weiterhin von Aufsichtsbehörden wie der MHRA und der FDA sowie den Therapieherstellern Vertex Pharmaceuticals und CRISPR Therapeutics überwacht.
Es bestehen jedoch immer noch Bedenken hinsichtlich der Sicherheit von CRISPR-basierten Therapien insgesamt. Es bestehen nämlich Bedenken hinsichtlich „Off-Target“-Effekten, die auftreten, wenn Cas9 auf andere Teile des Genoms einwirkt, die sich nicht verändern sollten, und so unerwünschte Nebenwirkungen verursacht.
„Es ist bekannt, dass CRISPR zu falschen genetischen Veränderungen mit unbekannten Folgen für die behandelten Zellen führen kann“, sagte David Rueda, Leiter der Abteilung für molekulare und zelluläre Biophysik am Imperial College London, gegenüber dem UK Science Media Centre. „Wir müssen die gesamten Genomsequenzierungsdaten dieser Zellen sehen, bevor wir Schlussfolgerungen ziehen können“, sagte er. Dabei wird die gesamte DNA in den von Kasgewi bearbeiteten Zellen untersucht, um festzustellen, ob es zu unerwünschten Effekten kommt.
Im November 2023 hat das Vereinigte Königreich Casgevy für Menschen über 12 Jahre mit Sichelzellenanämie oder transfusionsabhängiger Beta-Thalassämie zugelassen. Im Dezember genehmigte die FDA die Behandlung für Menschen ab 12 Jahren mit Sichelzellenanämie, und im Januar 2024 genehmigte die Behörde Casgevy für Menschen mit transfusionsabhängiger Beta-Thalassämie in derselben Altersgruppe.
Die Behandlung wird derzeit von der Europäischen Arzneimittel-Agentur der Europäischen Union und der saudi-arabischen Lebensmittel- und Arzneimittelbehörde geprüft, so dass andere Länder Casgevy laut Vertex bald zulassen könnten.
Es ist unklar, wann Casgevy verfügbar sein wird, aber seine Reichweite wird weitgehend von seinen Kosten abhängen. Gentherapie kann Millionen von Dollar kosten, und es sieht so aus, als ob Casgevy keine Ausnahme sein wird. Dies kann dazu führen, dass es für viele Menschen, die es benötigen, unerreichbar ist.
„Das Problem besteht darin, dass diese Behandlungen sehr teuer sein werden. Der Schlüssel liegt also darin, sie auf der ganzen Welt breiter verfügbar zu machen“, sagte Kay Davies, Professor für Anatomie an der Universität Oxford, gegenüber dem British Science Media Centre.
Ein Sprecher von Vertex sagte gegenüber Nature, dass das Unternehmen noch keinen Preis für Casgevy in Großbritannien festgelegt habe, aber „mit den Gesundheitsbehörden zusammenarbeite, um die Erstattung und den Zugang des Arzneimittels für berechtigte Patienten so schnell wie möglich sicherzustellen“.
Laut STAT News entwickelt Intellia Therapeutics CRISPR-Therapien zur Behandlung von Erbkrankheiten im Körper. Darüber hinaus wird eine modifizierte Version von CRISPR namens „Base Editing“, die auf einzelne DNA-Bausteine abzielen kann, als Möglichkeit zur Behandlung von Krankheiten getestet. Beispielsweise testet Verve Therapeutics eine solche experimentelle Behandlung von Herzerkrankungen. Eine weitere vielversprechende neue Therapieart namens „Base Editing“ umfasst CRISPR, umfasst aber auch „zusätzliche Enzyme und genetische Anweisungen zum Einfügen, Löschen oder Umschreiben kurzer DNA-Segmente“, berichtet STAT News.
Erste Erkenntnisse deuten darauf hin, dass CRISPR eine häufige Form der erblichen Blindheit behandeln könnte. In einer kleinen Studie stellten einige Menschen mit angeborenem Sehverlust nach der Behandlung mit CRISPR eine Verbesserung des Sehvermögens fest.
Erste klinische Studien deuten darauf hin, dass eine direkt in das Auge injizierte CRISPR-Therapie bei der Behandlung der häufigsten Form des erblichen Sehverlusts bei Kindern vielversprechend sein könnte.
Diese Form des Sehverlusts, Leber angeborene Amaurose (LCA) genannt, tritt häufig bei der Geburt auf und ist auf eine Funktionsstörung oder den Tod lichtempfindlicher Zellen, sogenannter Photorezeptoren, in der Netzhaut im hinteren Teil des Auges zurückzuführen. Solche Probleme entstehen durch Mutationen in einem von mindestens 20 Genen.
Einige der häufigsten Ursachen für LCA sind Mutationen im Gen, das für das zentrosomale Protein 290 (CEP290) kodiert. Mehr als drei Viertel der Erkrankten tragen eine spezifische Mutation, die CEP290 beeinflusst, was für die ordnungsgemäße Funktion der Photorezeptoren von entscheidender Bedeutung ist.
Derzeit gibt es keine Heilung für LCA – aber es gibt inzwischen Hinweise darauf, dass das berühmte Gen-Editing-Tool CRISPR sicher eingesetzt werden kann, um das Sehvermögen mancher Menschen mit dieser Erkrankung zu verbessern. Die Ergebnisse der frühen Phase der Studie wurden im New England Journal of Medicine veröffentlicht.
Die Studie ist auch deshalb bemerkenswert, weil sie die erste Person umfasste, die jemals eine CRISPR-basierte Behandlung direkt im Körper erhielt. Im Vergleich dazu besteht die erste zugelassene CRISPR-Therapie darin, dem Körper Zellen zu entnehmen, sie im Labor zu bearbeiten und sie dann dem Patienten zurückzugeben.
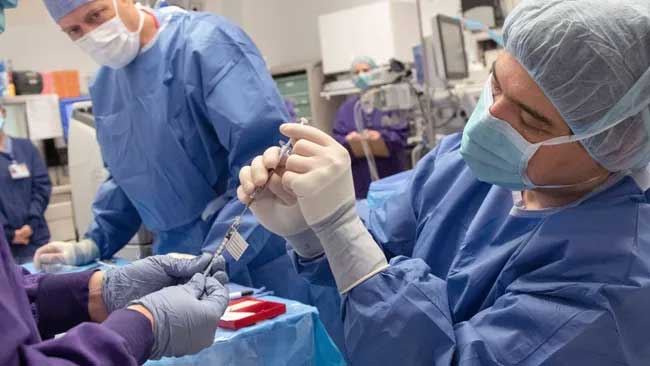
Hier führen Chirurgen des Casey Eye Institute der OHSU im Rahmen einer kürzlich durchgeführten klinischen Studie eine CRISPR-Genbearbeitung im Körper durch. OHSU/Kristyna Wentz-Graff
An der Studie nahmen 14 Personen teil – 12 Erwachsene und zwei Kinder. Sie alle hatten eine spezifische Mutation im CEP290-Gen, von der die meisten LCA-Patienten betroffen sind. Die Teilnehmer erhielten eine Injektion eines CRISPR-Medikaments namens EDIT-101 in das Auge mit dem stärksten Sehverlust. Das andere Auge diente zum Vergleich.
EDIT-101 enthält winzige Leitfäden, die „molekulare Scheren“ – sogenannte Cas9-Enzyme – zum mutierten CEP290-Gen führen. Die Schere schneidet den defekten Teil des Gens heraus und stellt so dessen Funktion wieder her.
Das Team verwendete eine CRISPR-basierte Strategie, da CEP290 ein großes Gen ist, was es zu einem schwierigen Ziel für die traditionelle Gentherapie macht. Einige Gentherapien verwenden modifizierte Viren, um funktionsfähige Gene in Zellen einzuschleusen, um fehlerhafte Gene zu ersetzen. Das CEP290-Gen ist jedoch zu groß, um in ein solches Abgabesystem zu passen.
Nach dieser Behandlung wurden alle Teilnehmer einem Sehtest unterzogen, der ein Jahr lang alle drei Monate durchgeführt wurde, gefolgt von einer selteneren Überwachung für zwei Jahre. Am Ende des Testzeitraums zeigten 11 der 14 Freiwilligen messbare Verbesserungen bei mindestens einem Sehtest, während sechs bei zwei oder mehr Tests Verbesserungen verzeichneten. Ein Studienteilnehmer teilte mit, dass er sein Telefon wiederfinden konnte, wenn er es verlor, und dass er die kleinen Lichter an seiner Kaffeemaschine sehen konnte, was ihm vor der Behandlung nicht möglich war.
Diejenigen, die keine messbaren Verbesserungen zeigten, befanden sich tendenziell in einem späteren Stadium der Krankheit, in dem ihre Zellen zu Beginn ein hohes Maß an Funktionsstörungen aufwiesen, stellten die Studienteilnehmer fest. Bei keinem der Teilnehmer traten durch die Behandlung unerwünschte Nebenwirkungen auf.
Obwohl EDIT-101 Zellen behandeln kann, die in der Netzhaut vorhanden sind, kann es den Verlust bereits abgestorbener Zellen nicht rückgängig machen. Dies bedeutet, dass bei den Teilnehmern zwar eine gewisse Verbesserung des Sehvermögens zu verzeichnen ist, dieses jedoch weiterhin eingeschränkt bleibt.
Der nächste Schritt wird darin bestehen, die Therapie an weiteren Patienten zu testen. Das Team hofft insbesondere, das Medikament an jüngeren Patienten testen zu können, von denen wir hoffen, dass sie noch bessere Ergebnisse erzielen.
Der Nobelpreis für Chemie 2020 ging an zwei Frauen, die ein Gen-Editing-Tool namens CRISPR-Cas9 entwickelt haben, das DNA wie eine molekulare Schere schneidet.
Die Technologie „hat nicht nur die Grundlagenforschung revolutioniert, sondern auch innovative Nutzpflanzen hervorgebracht und wird zu bahnbrechenden neuen Behandlungen führen“, sagte Klaas Gustafsson, Vorsitzender des Nobelkomitees für Chemie, in einer Erklärung. Mit der Fähigkeit, bestimmte DNA-Sequenzen geschickt aus dem Genom herauszuschneiden, können Wissenschaftler die Genfunktion genau bestimmen; Diese Entdeckungen tragen nicht nur zu unserem grundlegenden Verständnis der Funktionsweise dieser Gene bei, sondern können auch praktische Anwendungen haben, etwa für den Anbau dürre- und schädlingsresistenter Pflanzen und die Entwicklung von Behandlungen für Krebs und genetische Krankheiten. Das genetische Cut-and-Paste-System wird auch in neuen COVID-19-Diagnosetests eingesetzt.
Der Nobelpreis für ihre Entwicklung der Genombearbeitung ging an Emmanuelle Charpentier, Leiterin der Pathogenforschungseinheit der Max-Planck-Gesellschaft, und Jennifer Doudna, Professorin für Biochemie, Biophysik und Strukturbiologie an der University of California, Berkeley. Laut Science Magazine ist dies der erste wissenschaftliche Nobelpreis, der an ein rein weibliches Team verliehen wird.
Laut einer Erklärung des Nobelkomitees begann die Entwicklung von CRISPR-Cas9 zufällig, als Charpentier das Bakterium Streptococcus pyogenes untersuchte, das eine Reihe von Krankheiten von Mandelentzündung bis hin zu Sepsis verursacht. Charpentier entdeckte, dass die Bakterien ein Molekül namens tracrRNA enthalten, das S. pyogenes vor einer Infektion durch Viren schützt, wie aus einem Bericht in der Zeitschrift Nature aus dem Jahr 2011 hervorgeht.
Es stellt sich heraus, dass tracrRNA nur eine Komponente eines größeren Abwehrmechanismus ist, der als CRISPR/Cas-System bekannt ist und mit dem Bakterien die DNA von Viren, die sie infizieren wollen, zerschneiden und abbauen. Nach einem Virusangriff bauen Bakterien einen Teil der viralen DNA in ihr eigenes Genom ein; Diese Kampfbeute reihen sich im gesamten Genom aneinander, tauchen immer wieder auf und werden als „Cluster regelmäßig beabstandeter kurzer palindromischer Wiederholungen“ bezeichnet, abgekürzt als CRISPR. Diese archivierten Gene sollen Bakterien dabei helfen, Viren zu erkennen und künftige Angriffe abzuwehren.
Um jedoch zunächst die virale DNA zu schneiden, verwenden Bakterien „CRISPR-assoziierte“ Proteine, sogenannte Cas-Proteine, gesteuert durch tracrRNA und andere Moleküle.
Nach der Entdeckung von tracrRNA begann Charpentier mit Doudna zusammenzuarbeiten und die beiden stellten die genetische Schere von Bakterien in einem Reagenzglas nach. In ihrer bahnbrechenden Arbeit, die 2012 in der Fachzeitschrift „Science“ veröffentlicht wurde, vereinfachten sie das System zu einem praktischen Werkzeug zur Genbearbeitung, das in der Lage ist, spezifische DNA-Sequenzen aus dem Genom anzusprechen und auszuschneiden. Das Tool wurde seitdem weiter verfeinert und für eine Vielzahl von Anwendungen eingesetzt, einschließlich der jüngsten Entwicklung von Diagnosetests für COVID-19, berichtet die BBC.
„Diese Entdeckung, die ursprünglich auf dem natürlichen Abwehrmechanismus von Bakterien gegen Viren beruhte, wird unzählige Anwendungen bei der Behandlung und Heilung genetischer Krankheiten und im Kampf gegen Krebs haben und sich auch auf die Landwirtschaft und andere Bereiche auswirken“, sagte Louis Echegoyen, Präsident von sagte in einer Erklärung der American Chemical Society. „Die Zukunft dieser Technologie ist wirklich rosig und vielversprechend.“
Einige Wissenschaftler hatten erwartet, dass der Biochemiker Feng Zhang vom Broad Institute den Nobelpreis mit Charpentier und Doudna teilen würde, weil er kurz nach ihrer Entdeckung zeigte, dass CRISPR auch in Säugetierzellen funktioniert, berichtet das Science Magazine. Basierend auf Zhangs Arbeit erhielt das Broad Institute das erste Patent für den Einsatz der CRISPR-Genbearbeitungstechnologie in Eukaryoten – komplexen Zellen mit Kernen zur Speicherung von DNA –, aber die Institute Charpentier und Doudna kämpfen laut The Scientist weiterhin um ihre eigenen Patente.