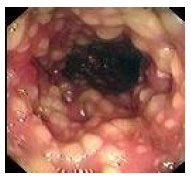
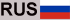La superbacteria Clostridioides difficile, o C. diff, puede causar infecciones intestinales peligrosas. Existen opciones de tratamiento limitadas y los pacientes a menudo experimentan una reinfección, que puede ser fatal. Ahora, una nueva investigación muestra que esta peligrosa bacteria puede desarrollar rápidamente resistencia a los antibióticos, aunque esta resistencia tiene un costo para la propia superbacteria. Los investigadores han identificado dos mecanismos distintos de resistencia a los medicamentos en C. difficile.
Las toxinas producidas por las cepas de Clostridioides difficile en el tracto gastrointestinal causan colitis pseudomembranosa, generalmente después del uso de antibióticos. Los síntomas incluyen diarrea, a veces con sangre, que rara vez progresa a megacolon tóxico, perforación del colon, sepsis y abdomen agudo.
Según los autores del estudio, los hallazgos resaltan la necesidad de un seguimiento cuidadoso de la resistencia bacteriana a los antibióticos, especialmente en los hospitales.
Para la mayoría de las personas, las bacterias beneficiosas que viven en los intestinos los protegen de las infecciones. Cuando estas bacterias mueren (por ejemplo, como resultado de un tratamiento con antibióticos para una infección no relacionada), el colon se vuelve vulnerable y es entonces cuando C. difficile lo ataca. Las personas que están tomando o han tomado antibióticos recientemente tienen 10 veces más probabilidades de infectarse con C. difficile que aquellas que no los han tomado. Otros factores de riesgo incluyen estar en un hospital o en un asilo de ancianos, tener un sistema inmunológico debilitado o ser muy joven o muy mayor.
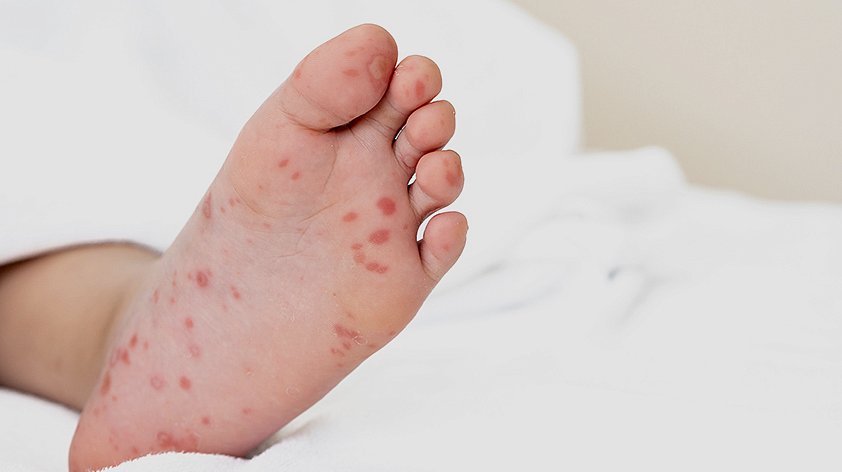
colitis pseudomembranosa
Desafortunadamente, sólo hay tres antibióticos disponibles para tratar las infecciones por C. difficile. La vancomicina es el fármaco de elección para la mayoría de los pacientes, pero en aproximadamente un tercio de los pacientes la infección regresa al mes de finalizar el tratamiento. Una posible razón para esto, sugirieron los autores del estudio, es que C. difficile evoluciona para resistir la vancomicina.
“No sabemos si circulan cepas resistentes y causan infecciones humanas porque los laboratorios hospitalarios no realizan pruebas de resistencia a la vancomicina”, dijo a Live Science la autora del estudio Jessica Buddle, estudiante de doctorado de la Universidad de Sheffield en el Reino Unido. “Ha habido sólo unos pocos informes de resistencia en todo el mundo. Sin embargo, dada la falta de pruebas, es probable que esta no sea toda la historia”.
Para saber si las bacterias podrían desarrollar resistencia a la vancomicina, los investigadores modificaron genéticamente dos poblaciones de C. difficile: una con una tasa de mutación normal y otra que evolucionó más rápido. Para el nuevo estudio, publicado el 15 de agosto en la revista PLOS Biology, cultivaron cinco cepas de cada población en presencia de concentraciones crecientes de vancomicina.
En cuatro días, nueve de las diez cepas desarrollaron resistencia a la vancomicina; al final del experimento de 60 días, las 10 cepas pudieron crecer con 32 veces la cantidad de vancomicina que normalmente se usa para tratar las infecciones por C. difficile.
Aunque las bacterias utilizaron varias mutaciones genéticas diferentes para escapar de la vancomicina, todas las cepas resistentes tenían una cosa en común: no podían crecer tan rápido como C. difficile, que no desarrolló resistencia a la vancomicina. Además, varias cepas eran más pequeñas o tenían dificultades para producir esporas, que la bacteria utiliza para sobrevivir y propagarse en el medio ambiente.
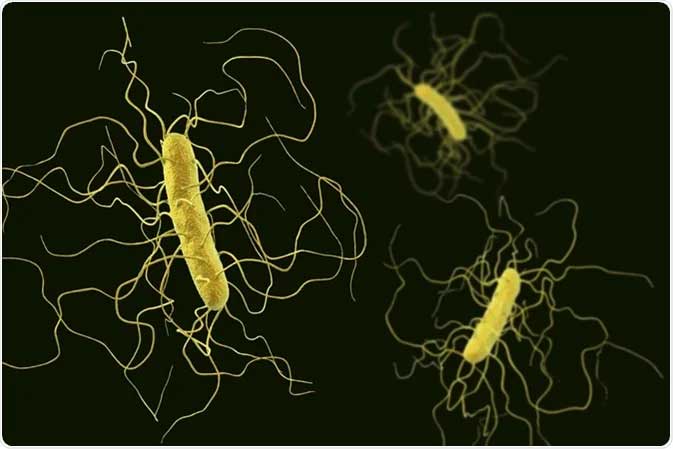
Clostridium difficile
“En este estudio, la resistencia que C. difficile desarrolla a la vancomicina es contraproducente porque también parece reducir la capacidad de la bacteria para sobrevivir de otras maneras”, dijo a WordsSideKick.com el Dr. Paul Feuerstadt, gastroenterólogo y profesor clínico de medicina. en un correo electrónico en la Facultad de Medicina de Yale en Connecticut. Esta puede ser la razón por la que la alta resistencia a la vancomicina no es tan común en C. difficile como en otras bacterias, añadió.
Sin embargo, comprender y prevenir la resistencia a los antibióticos es fundamental para garantizar la tratabilidad de las infecciones por C. difficile.
Saber cómo C. difficile resiste los antibióticos permite a los científicos desarrollar nuevos tratamientos que son más difíciles de resistir, dijo Feuerstadt, que no participó en el estudio. Eliminar las infecciones de forma rápida y eficaz no sólo evita que las bacterias se vuelvan resistentes, sino que también significa que no pueden sobrevivir el tiempo suficiente para desarrollar un crecimiento más rápido o una mejor transmisión.
“Identificar el problema de la resistencia significará que tomaremos las decisiones correctas en futuras recomendaciones de tratamiento”, dijo Buddle. “Si utilizamos el fármaco adecuado para tratar la infección y completamos el tratamiento completo según lo prescrito, aumentamos las posibilidades de eliminar con éxito la infección y reducir el riesgo de resistencia. Necesitamos tratar a los antibióticos como un recurso valioso y todos deben hacer su parte”.
Mientras tanto, las bacterias resistentes a los antibióticos podrían matar a más de 39 millones de personas en los próximos 25 años, según un estudio realizado por un equipo internacional de científicos publicado en un artículo de la revista médica Lancet.
“Estimamos que para 2050 habrá 1,91 millones de muertes relacionadas con la RAM cada año en todo el mundo y 8,22 millones de muertes relacionadas con la RAM. En conjunto, de 2025 a 2050, nuestro escenario de referencia proyecta 39,1 millones de muertes atribuibles a la RAM y 169 millones de muertes atribuibles a la RAM”, afirma el artículo.
Los científicos predicen que el mayor número de muertes se producirá en el sur y el este de Asia, así como en Oceanía y el África subsahariana.
Los patógenos bacterianos a los que los antibióticos no responden se denominan resistentes o superbacterias. Según las estadísticas de la OMS, las infecciones relacionadas son la tercera causa de muerte en el mundo después de las enfermedades cardíacas y los accidentes cerebrovasculares. En 2019, 4,95 millones de personas murieron a causa de ellos. La mayor preocupación es el Staphylococcus aureus, que es resistente a la meticilina y otros antibióticos.
Clostridia difficile (lat. Clostridioides difficile, nombre tradicional Clostridium difficile, sinónimo Peptoclostridium difficile) es una especie de bacteria ubicua. Las infecciones por Clostridioides difficile son una de las principales causas de diarrea y mortalidad en los hospitales.
Hasta hace poco, la especie Clostridium difficile pertenecía al género Clostridium, que se incluye en la familia Clostridiaceae, orden Clostridiales, clase Clostridia y se llamaba Clostridium difficile. Recientemente, el lugar de esta especie en la taxonomía de bacterias ha cambiado varias veces, se reclasificó en el género Peptoclostridium, se le dio el nombre de Peptoclostridium difficile, y en 2016 se transfirió al género recién organizado Clostridioides, que se incluyó en la familia. Peptostreptococcaceae, el mismo orden Clostridiales y clase Clostridia, filo Firmicutes, <grupo sin rango> grupo Terrabacteria, reino Bacteria y por lo tanto pasó a ser conocido como Clostridioides difficile (un nombre equivalente válido es Clostridium difficile).
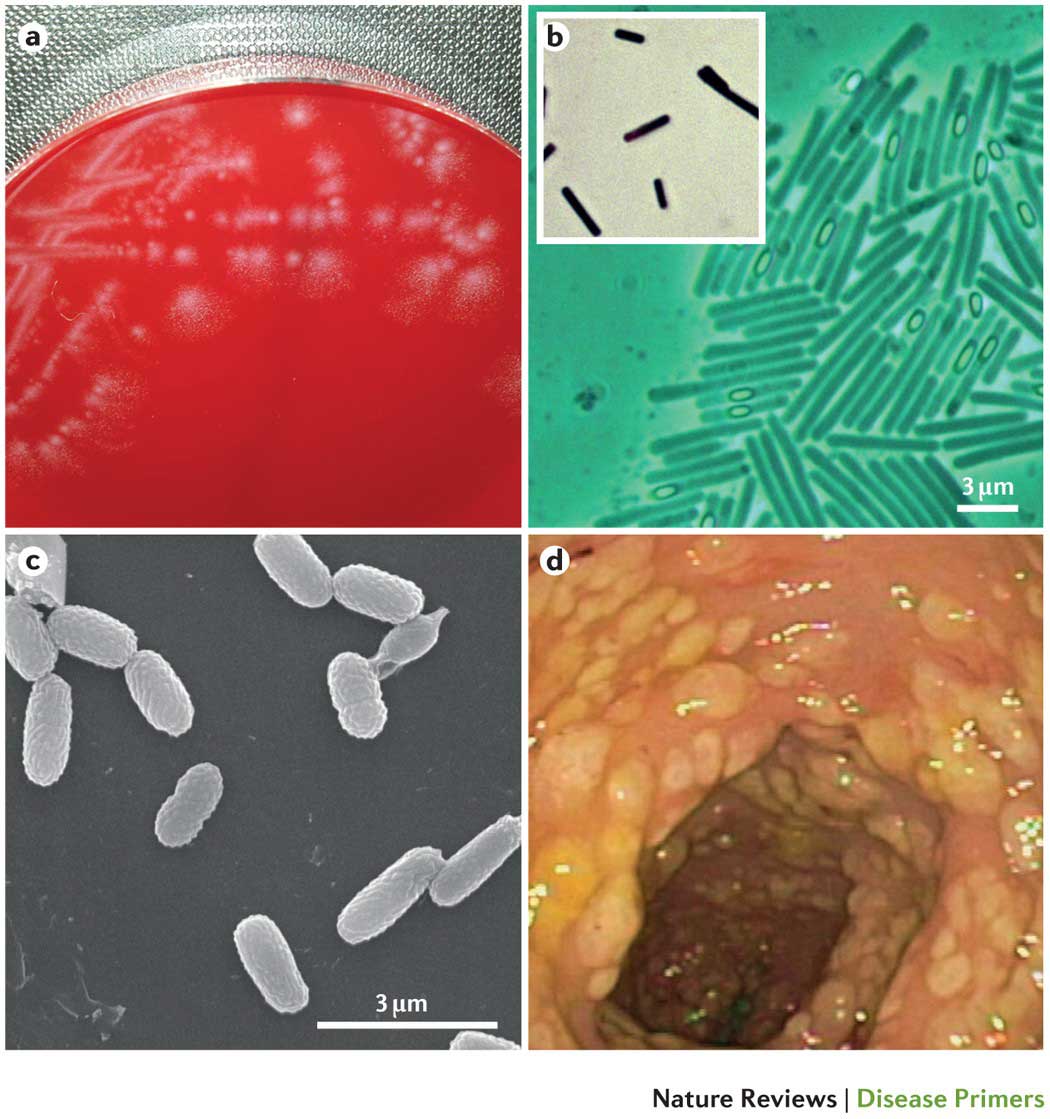
Infección por Clostridium difficile
Los Clostridioides difficile son bacterias grampositivas, formadoras de esporas, estrictamente anaeróbicas, con forma de grandes bastones alargados con un bulto en el medio. Clostridioides difficile puede sobrevivir durante mucho tiempo en el ambiente externo. Sus esporas son resistentes al tratamiento térmico. Clostridioides difficile es naturalmente resistente a la mayoría de los antibióticos.
Las cepas toxigénicas de Clostridioides difficile producen varios factores patogénicos. Los más estudiados entre ellos son:
– toxina A (enterotoxina)
– toxina B (citotoxina)
– una proteína que inhibe la motilidad intestinal
Clostridium difficile forma parte de la microflora normal del tracto gastrointestinal (colona principalmente el intestino grueso, pero puede encontrarse en el intestino delgado y la cavidad bucal), el tracto genital femenino y, en ocasiones, la piel. Clostridium difficile está presente en los intestinos de aproximadamente la mitad de los recién nacidos y en entre el 3 y el 15% de los niños sanos mayores de 2 años y los adultos. La cantidad de Clostridium difficile en la microflora intestinal normal de un adulto sano no supera el 0,01-0,001%. Sin embargo, cuando se toman antibióticos, esta última cifra puede aumentar hasta un 15-40%.
La diarrea asociada a antibióticos (DAA) es una de las complicaciones que ocurre en entre el 5 y el 25% de los pacientes que toman antibióticos. Clostridium difficile no es la única causa de DAA, aunque es bastante común (aproximadamente un tercio de los casos). La DAA también puede ser causada por Salmonella spp., Clostridium perfringens tipo A, Staphylococcus aureus, Klebsiella oxytoca, hongos cándida y otros microorganismos. La DAA es una de las infecciones nosocomiales más extendidas. Sólo en EE.UU. se registran anualmente hasta 1 millón de casos de DAA. A pesar de la importante portación de Clostridium difficile, los bebés prácticamente no padecen DAA causada por Clostridium difficile.
La aparición de DAA se debe al hecho de que los antibióticos suprimen no solo la microflora intestinal patógena, sino también la normal, lo que en condiciones normales evita que se multipliquen los microorganismos patógenos y oportunistas. Como resultado del efecto de los antibióticos sobre la microflora normal, el número de microbios patógenos y oportunistas resistentes a los medicamentos (incluido Clostridium difficile) en el cuerpo humano puede aumentar significativamente.
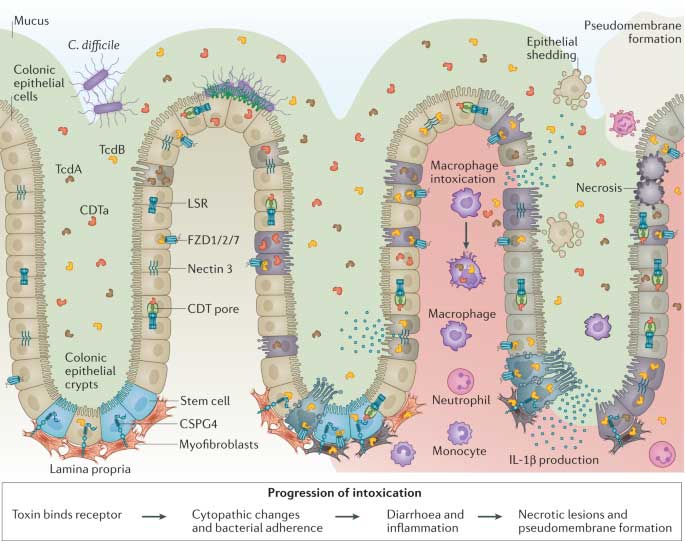
Toxinas de Clostridioides difficile: mecanismos de acción y terapéutica antitoxina
La causa de la DAA puede ser casi cualquier agente antimicrobiano, pero la incidencia de la enfermedad depende significativamente del tipo de antibiótico (y es casi independiente de la dosis). La mayoría de las veces, la DAA es causada por la ingesta de clindamicina, cefalosporinas y ampicilina.
Las manifestaciones de la DAA varían desde diarrea leve hasta enterocolitis grave llamada “colitis pseudomembranosa”. La causa de la colitis pseudomembranosa en la gran mayoría de los casos es la infección por Clostridium difficile.
El principal factor de riesgo para la aparición de formas graves de DAA causadas por Clostridium difficile es la terapia con antibióticos. Incluso una dosis única de un antibiótico de amplio espectro, independientemente de la dosis y la vía de administración, puede provocar el desarrollo de DAA y colitis pseudomembranosa. También es un factor de riesgo una estancia hospitalaria prolongada, especialmente en la misma sala con portadores de Clostridium difficile.
La colitis pseudomembranosa se caracteriza por diarrea acuosa frecuente y profusa, a veces mezclada con sangre, moco y pus. Como regla general, la diarrea se acompaña de fiebre, temperatura elevada a 38,5-40°C, dolor abdominal moderado o intenso, tipo calambres o constante. La tasa de mortalidad en ausencia de tratamiento para pacientes con colitis pseudomembranosa es del 15 al 30%
Una característica de la infección por Clostridium difficile son sus frecuentes recaídas, en promedio del 20 al 25%, cuya causa está asociada con la presencia de esporas de Clostridium difficile en los intestinos o la reinfección. Por lo general, después del tratamiento, se produce recuperación o mejoría, pero entre los días 2 a 28 (en promedio, 3 a 7 días) se produce una recaída, idéntica al episodio inicial.
Diagnóstico y tratamiento de la DAA causada por Clostridium (Clostridioides) difficile
Los principales factores dañinos del cuerpo humano en las enfermedades causadas por Clostridium difficile son las toxinas A y B. No todas las cepas de Clostridium difficile producen estas toxinas. Para detectar la infección por cepas toxigénicas de Clostridium difficile, se realiza una prueba de heces para detectar la presencia de toxinas A y B o una prueba de heces: cultivo para Clostridium difficile. Normalmente, los resultados de la prueba deberían ser negativos.
Si se detecta DAA, se debe suspender el antibiótico que causó la enfermedad. El tratamiento de casos graves de DAA y colitis pseudomembranosa incluye terapia con vancomicina o metronidazol, a los que son sensibles la mayoría de las cepas de Clostridium difficile. No se permite tomar medicamentos antidiarreicos y antiespasmódicos debido al riesgo de desarrollar una complicación grave: el megacolon tóxico.
Un probiótico eficaz es Enterol, que contiene hongos de levadura liofilizados Saccharomyces boulardi, que tienen un efecto antimicrobiano directo no solo contra Clostridium difficile, sino también contra otros microorganismos que pueden causar DAA. Para prevenir el desarrollo de DAA y restaurar la microflora intestinal después de suspender un antibiótico (vancomicina o metronidazol), se utilizan medicamentos que contienen cepas de representantes de la microflora natural: Lactobacillus acidophilus, Lactobacillus rhamnosus, Bifidobacterium longum, Enterococcus faecium y otros (Linex, Bifiform, etc.).
La Organización Mundial de Gastroenterología destaca la eficacia del uso de la cepa Lactobacillus casei DN-114 001 para el tratamiento de la diarrea asociada a Clostridium difficile, así como para su prevención, las siguientes cepas probióticas (Probióticos y prebióticos. Recomendaciones prácticas):
– Lactobacillus casei DN-114 001 en leche fermentada con Lactobacillus bulgaricus y Streptococcus thermophilus 1010 UFC, 2 veces al día
– Lactobacillus acidophilus + Bifidobacterium bifidum (cepas especiales) – 2 x 1010 UFC cada uno, 1 vez al día
– Saccharomyces cerevisiae (boulardii). Edad 1 año – 2 x 1010 UFC por día
– Oligofructosa – 4 g, 3 veces al día, 4 g.
Agentes antibacterianos activos contra Clostridium difficile: vancomicina, metronidazol, rifaximina, tetraciclina, doxiciclina, lincomicina. Clostridium difficile es resistente a la ciprofloxacina. El 21 de octubre de 2016, la FDA de EE. UU. aprobó el uso en los Estados Unidos de un nuevo medicamento para prevenir las recaídas de la infección por Clostridium difficile en pacientes mayores de 18 años: bezlotoxumab, nombre comercial Zinplava. Bezlotoxumab es un anticuerpo monoclonal diseñado para neutralizar la toxina B de Clostridium difficile.