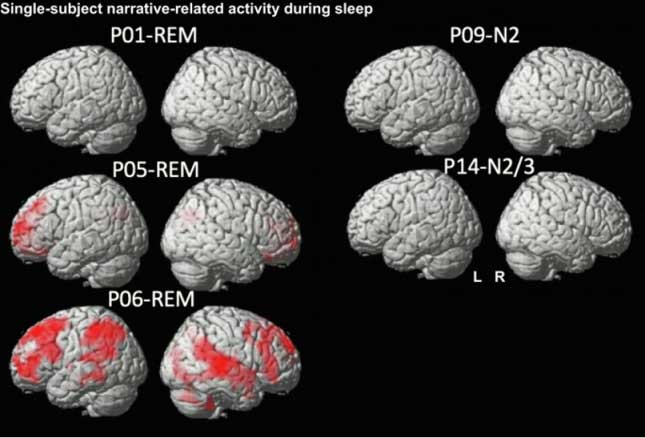
Los científicos han identificado decenas de miles de “nudos” misteriosos en el ADN humano que pueden desempeñar un papel clave en el control de la actividad genética. Se ha revelado la actividad del ADN de 4 cadenas en las células vivas. Se ha creado ADN sintético con cuatro letras extra. El ADN se retuerce adoptando formas extrañas para adaptarse a las células.
Los científicos han identificado decenas de miles de “nudos” misteriosos en el ADN humano que pueden desempeñar un papel clave en el control de la actividad genética. Conocer la ubicación precisa de estos ganglios, conocidos como “i-motifs”, podría conducir al desarrollo de nuevos tratamientos para enfermedades, incluido el cáncer, según los investigadores detrás del trabajo.
El ADN está formado por bloques de construcción llamados nucleótidos, cada uno de los cuales lleva una de las siguientes bases: adenina, guanina, timina o citosina. Estas bases son las letras individuales que componen el código de ADN. El ADN tiene una estructura de escalera y, por lo general, las bases de un lado de la escalera se emparejan con una pareja del otro lado, uniéndose en el medio para formar los peldaños de la escalera. La adenina se empareja con la timina y la guanina se empareja con la citosina.
Sin embargo, a veces las citosinas pueden emparejarse entre sí en lugar de con la guanina. Esto hace que la molécula de ADN se gire sobre sí misma, creando una estructura sobresaliente de cuatro hebras llamada i-motif.
Los investigadores descubrieron por primera vez i-motifs en células humanas en 2018. En ese momento, sospecharon que estos nodos podrían ser importantes reguladores del genoma, ayudando a controlar qué genes se activan o desactivan. Sin embargo, hasta ahora se sabía poco sobre dónde se encuentran exactamente estas estructuras nudosas y cuántas hay en el genoma humano.
En un nuevo estudio publicado el 29 de agosto en The EMBO Journal, los investigadores mapearon 50.000 i-motifs. Estos motivos i están ubicados en todo el genoma, pero normalmente ocurren en regiones del ADN que controlan la actividad genética, anotaron los autores del estudio.
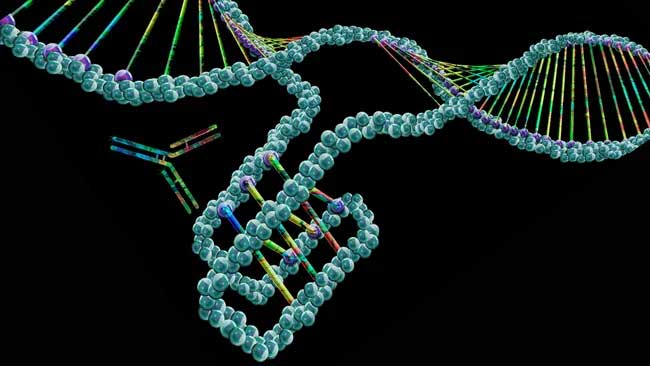
En el nuevo estudio, los científicos mapearon 50.000 estructuras similares a nudos en el ADN conocidas como “i-motivos”. KEITH CHAMBERS/BIBLIOTECA DE FOTOS DE CIENCIA
“Nuestros resultados confirman que los i-motifs no son sólo una curiosidad de laboratorio sino un fenómeno generalizado que probablemente desempeña un papel clave en la función del genoma”, dijo en un comunicado Daniel Christ, coautor del estudio y director del Centro de Terapias Dirigidas del Instituto. Investigación médica Garvan en Australia.
Christ y sus colegas descubrieron i-motifs en ADN extraído de células humanas en el laboratorio. Identificaron estos nodos utilizando anticuerpos diseñados para reconocer específicamente los i-motifs y formar complejos con ellos. Luego, el equipo purificó estos complejos anticuerpo-nodo para secuenciar el ADN que contienen.
“Descubrimos que los i-motifs están asociados con genes que son altamente activos durante ciertos períodos del ciclo celular”, dijo en un comunicado Cristian David Peña Martínez, autor principal del estudio y becario postdoctoral de Garvan. El ciclo celular es el proceso mediante el cual las células se replican en el cuerpo.
“Esto sugiere que desempeñan un papel dinámico en la regulación de la actividad genética”, añadió Peña Martínez.
El equipo también descubrió i-motivos en las regiones “promotoras” de varios genes relacionados con el cáncer. Los promotores son un tipo de material genético que enciende y apaga un gen determinado, como un interruptor de luz. En las células cancerosas, estos genes pueden desregularse, lo que lleva a una mayor división celular y al crecimiento característico de los tumores.
Este nuevo descubrimiento sugiere que los i-motifs algún día podrían convertirse en objetivos de medicamentos contra el cáncer, sugirió el equipo. Descubrieron i-motivos en la familia de genes MYC, que se sabe que está alterada en aproximadamente el 70% de los cánceres humanos.
“Esto representa una oportunidad emocionante para atacar genes asociados a enfermedades a través de la estructura i-motif”, dijo Peña Martínez. Por supuesto, se necesita más investigación para trasladar esta idea de la teoría a la práctica en pacientes con cáncer.
Se ha revelado la actividad del ADN de 4 cadenas en las células vivas. Dos hebras delgadas retorcidas juntas en una espiral es la forma icónica de la molécula de ADN. Pero a veces el ADN puede formar una rara hélice cuádruple, y esta extraña estructura puede desempeñar un papel en enfermedades como el cáncer.
No se sabe mucho sobre estos ADN de cuatro cadenas, conocidos como G-quadruplex, pero los científicos ahora han desarrollado una nueva forma de detectar estas extrañas moléculas y observar cómo se comportan en las células vivas. En un estudio publicado el 8 de enero de 2021 en la revista Nature Communications, el equipo describió cómo ciertas proteínas hacen que el G-quadruplex se deshaga; En el futuro, su trabajo podría conducir a nuevos fármacos que atrapen el ADN de cuatro cadenas e interrumpan su actividad. Las drogas pueden interferir, por ejemplo, cuando un ADN extraño promueve el crecimiento de un tumor canceroso.
“Existe una creciente evidencia de que los G-cuadruplex desempeñan un papel importante en una amplia variedad de procesos esenciales para la vida, así como en una serie de enfermedades”, dijo en un comunicado el autor del estudio, Ben Lewis, del Departamento de Química del Imperial College de Londres. .
En general, los cuádruplex G se producen con mucha más frecuencia en las células cancerosas que en las sanas, según el comunicado. Diversos estudios han relacionado la presencia de ADN de cuatro cadenas con la rápida división de las células cancerosas, proceso que conduce al crecimiento tumoral; Entonces, los científicos plantearon la hipótesis de que atacar el ADN extraño con medicamentos podría ralentizar o detener esta división celular desenfrenada. Algunos estudios ya apoyan esta idea.
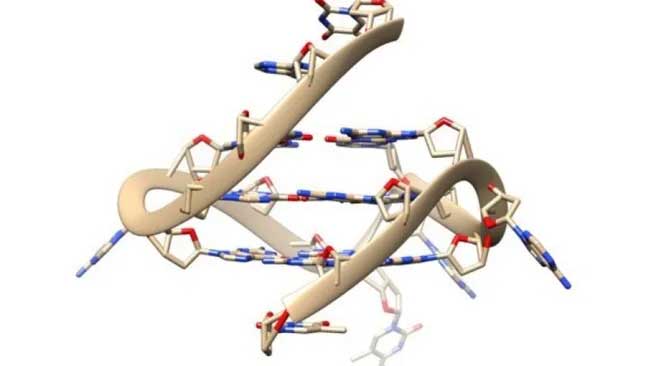
G-cuádruplex. Colegio Imperial de Londres
“Pero el eslabón perdido era obtener imágenes de esta estructura directamente en las células vivas”, dijo Lewis. En otras palabras, los científicos necesitaban una mejor manera de observar estas moléculas de ADN en acción. Nuevas investigaciones están comenzando a completar este conocimiento faltante.
Los G-cuadruplex pueden formarse cuando una única molécula de ADN de doble hebra se pliega sobre sí misma o cuando varias hebras de ADN se unen en un único ácido nucleico conocido como guanina, uno de los componentes básicos del ADN, según la revista Discover. Para detectar este ADN inusual en las células, el equipo utilizó una sustancia química llamada DAOTA-M2, que emite luz fluorescente cuando se une a los cuádruplex G. En lugar de simplemente medir el brillo de la luz, que cambia según la concentración de moléculas de ADN, el equipo también rastreó cuánto tiempo estuvo encendida la luz.
El seguimiento de cuánto tiempo permaneció la luz ayudó al equipo a ver cómo interactúan diferentes moléculas con el ADN de cuatro cadenas en las células vivas. Cuando la molécula se adhirió a una hebra de ADN, desprendió el brillante DAOTA-M2, lo que provocó que la luz se desvaneciera más rápido que si la sustancia química hubiera permanecido en su lugar. Utilizando estos métodos, el equipo identificó dos proteínas llamadas helicasas que desenrollan hebras de ADN de cuatro hebras y desencadenan el proceso de descomposición.
También identificaron otras moléculas que se unen al ADN; Los estudios futuros de estas interacciones moleculares pueden ayudar a los científicos a desarrollar fármacos que se unan al ADN.
“Muchos investigadores se han interesado en el potencial de las moléculas de unión del G-quadruplex como posibles fármacos para enfermedades como el cáncer”, afirma en un comunicado Ramon Vilar, profesor de química inorgánica medicinal del Imperial. “Nuestro método nos ayudará a avanzar en nuestra comprensión de estos posibles nuevos fármacos”.
Los investigadores crearon ADN sintético utilizando cuatro moléculas adicionales para que el producto resultante tuviera un código de ocho letras en lugar de cuatro. Con el aumento del número de letras, este ADN adquirió una capacidad mucho mayor para almacenar información. Los científicos llamaron al nuevo ADN “hachimoji”, que significa “ocho letras” en japonés, ampliando el trabajo previo de diferentes grupos que crearon ADN similar usando seis letras.
Un estudio publicado el 20 de febrero de 2019 en la revista Science confirma esta última suposición: recientemente los científicos formaron un nuevo tipo de ADN con una elegante estructura de doble hélice y descubrieron que tiene propiedades que pueden sustentar la vida.
El ADN natural está formado por cuatro moléculas llamadas bases nitrogenadas que se unen para formar el código de la vida en la Tierra: A se une a T; G se une a C. El ADN de Hachimoji incluye estas cuatro bases naturales, así como cuatro bases de nucleótidos sintéticas más: P, B, Z y S.
El equipo de investigación, que incluyó varios equipos diferentes en los Estados Unidos, creó cientos de estas dobles hélices de Hachimoji con diferentes combinaciones de pares de bases de nucleótidos naturales y sintéticos. Luego llevaron a cabo una serie de experimentos para descubrir si varias dobles hélices tenían las propiedades necesarias para sustentar la vida.
El ADN natural tiene una propiedad distintiva que ninguna otra molécula genética parece tener: es estable y predecible. Esto significa que los investigadores pueden calcular exactamente cómo se comportará en determinadas temperaturas y entornos, incluido cuándo comenzará a degradarse.
Pero resulta que los investigadores pudieron hacer lo mismo con el ADN de Hachimoji: pudieron desarrollar un conjunto de reglas que podrían predecir la estabilidad del ADN cuando se expone a diferentes temperaturas.
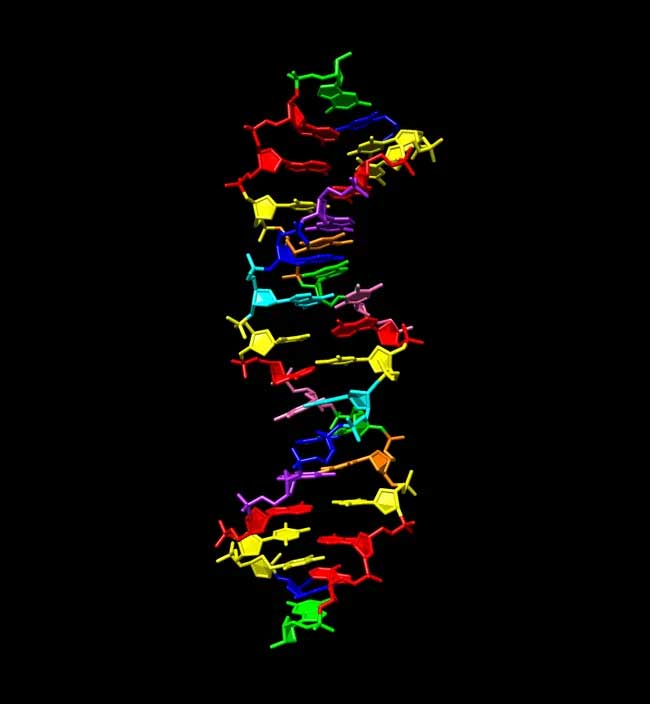
Los investigadores han desarrollado en el laboratorio un nuevo tipo de ADN que consta de ocho letras en lugar de las cuatro naturales. Millie Georgiadis, Facultad de Medicina de la Universidad de Indiana
Pero crear ADN que almacene información no es suficiente. También debe poder transmitir esta información a su molécula hermana, el ARN, para que este pueda luego ordenar a las proteínas que hagan todas las cosas en el cuerpo.
Con esto en mente, los investigadores desarrollaron enzimas sintéticas (proteínas que facilitan la reacción) que copiaron con éxito el ADN de Hachimoji en ARN de Hachimoji. Además, descubrieron que la molécula de ARN puede plegarse en forma de L, lo cual es necesario para una mayor transferencia de información.
Además, las hebras de ADN deben poder retorcerse formando la misma estructura tridimensional: la famosa doble hélice.
El equipo creó tres estructuras cristalinas del ADN de Hachimoji, cada una con una secuencia diferente de ocho pares de bases, y descubrió que cada una de ellas formaba una doble hélice clásica.
Sin embargo, para que el ADN de Hachimoji pueda sustentar la vida, existe un quinto requisito, dijo Benner. Es decir, debe ser autosuficiente o poder sobrevivir por sí solo. Sin embargo, los investigadores no investigaron este paso para evitar que la molécula se convirtiera en un peligro biológico que algún día podría colarse en los genomas de los organismos de la Tierra.
Además de proporcionar información sobre alternativas a la vida en el espacio, esta cadena de ADN de ocho letras también tiene aplicaciones en nuestro planeta. El alfabeto genético de ocho letras almacenaría más información y se uniría a ciertos objetivos de manera más específica, dijo Benner. Por ejemplo, el ADN de Hachimoji podría usarse para unirse a células de cáncer de hígado o toxinas de ántrax, o usarse para acelerar reacciones químicas.
“A medida que el número de letras aumenta de seis a ocho, la diversidad de secuencias de ADN aumenta significativamente”, escribió en Ichiro Hirao, biólogo molecular sintético del Instituto A*STAR de Bioingeniería y Nanotecnología en Singapur, que tampoco participó en el estudio. un correo electrónico. (Sin embargo, el grupo de Hirao también participó en un estudio anterior que creó cadenas de ADN de seis letras)
Por supuesto, “esta es sólo la primera demostración” de la doble hélice de ocho letras del ADN, y para uso práctico necesitamos mejorar la precisión y eficiencia de la replicación y transcripción en ARN, dijo Hirao en un correo electrónico. Sugiere que eventualmente podrán ampliar el número de letras aún más.
En 2021, los científicos capturaron un video de alta definición que mostraba que el ADN tomaba formas extrañas para introducirse dentro de las células.
En 1952, Rosalind Franklin tomó la primera fotografía indirecta del ADN estudiando cómo los rayos X rebotan en estas moléculas fundamentales. Pero no fue hasta 2012 que los científicos tomaron una fotografía directa del ADN utilizando un microscopio electrónico. Ahora, un equipo de investigadores del Reino Unido ha capturado vídeos de alta definición del ADN en movimiento, utilizando una combinación de microscopía avanzada y modelado.
Las células humanas contienen aproximadamente 6,6 pies (2 metros) de ADN. Dado que las células humanas son del orden de micrómetros, el ADN debe ser realmente bueno para “superenrollarse”, o doblarse y plegarse para compactarse firmemente dentro de la célula. Pero hasta hace poco, la tecnología no era lo suficientemente buena como para que los científicos vieran claramente cómo se ve la estructura del ADN en un estado superenrollado, escriben los autores en el estudio.
Para responder a esta pregunta, los autores del nuevo estudio recurrieron a “minicírculos de ADN” aislados y diseñados a partir de bacterias. Estas estructuras circulares de ADN también se encuentran en células humanas y su función se desconoce en gran medida. Los investigadores utilizaron estas estructuras de anillos porque los científicos pueden torcerlos de una manera que no funcionaría con hebras largas, la forma más común de ADN, según el comunicado.
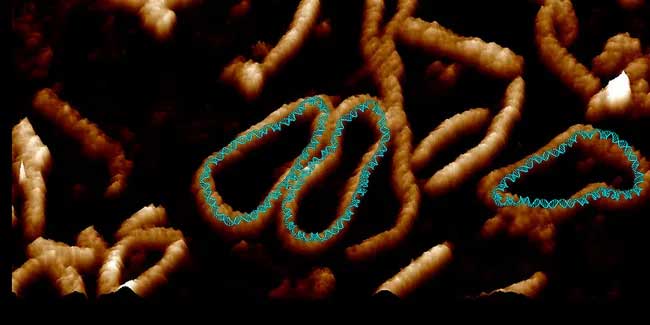
ADN. universidad de leeds
Para observar los movimientos en detalle, los investigadores utilizaron una combinación de simulaciones de supercomputadora y microscopía de fuerza atómica, en la que una punta afilada se desliza por la superficie de una molécula y mide las fuerzas que repelen la punta para delinear la estructura.
“Ver para creer, pero con un objeto tan pequeño como el ADN, ver la estructura helicoidal de toda la molécula de ADN era extremadamente difícil”, dijo la autora principal del estudio Alice Pyne, profesora de polímeros y materia blanda en la Universidad de Sheffield en el Reino Unido. quien registró los nuevos datos, dijo en un comunicado Marcos. “Los vídeos que desarrollamos nos permiten observar la torsión del ADN con un nivel de detalle nunca antes observado”.
Las imágenes del microscopio eran tan detalladas que se podía ver la estructura de doble hélice del ADN. Después de que los investigadores combinaron estas imágenes con simulaciones, pudieron ver la posición de cada átomo en el ADN a medida que se movía, según el comunicado.
Curiosamente, el ADN en su forma relajada apenas se movía. Pero cuando se retorcía, como suele ocurrir cuando se presiona en una célula, el ADN se transformaba en muchas otras formas, según el comunicado. Estas diferentes formas afectaron la forma en que la molécula de ADN interactuaba y se unía con otras moléculas de ADN a su alrededor, escriben los autores en el artículo.
Lynn Zechidrich, profesora de la Facultad de Medicina Baylor de Houston, Texas, que proporcionó los minianillos para el estudio, descubrió previamente cómo utilizar estas estructuras de anillos como vectores para la terapia génica insertando pequeños mensajes genéticos en los anillos.
Los científicos que realizaron el estudio “han desarrollado una técnica que muestra con gran detalle cuán arrugados, burbujeantes, curvados, desnaturalizados y de formas extrañas son”, dijo Zechidrich, que no participó directamente en el estudio, en un comunicado. “Necesitamos comprender cómo el superenrollamiento, que es tan importante para la actividad del ADN en las células, afecta al ADN, con la esperanza de que algún día aprendamos a imitarlo o controlarlo”.