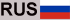La terapia génica se ha convertido en una gran noticia en los últimos años, en parte debido al rápido desarrollo de biotecnologías que permiten a los médicos llevar a cabo este tipo de tratamientos. En términos generales, la terapia génica es una técnica utilizada para tratar o prevenir enfermedades cambiando el contenido del ADN o la expresión de las células, a menudo reemplazando genes defectuosos por genes funcionales.
El término “terapia génica” aparece a veces con información errónea sobre las vacunas de ARNm, que incluyen las vacunas COVID-19 de Pfizer y Moderna. Estas vacunas contienen ARNm, un primo genético del ADN, que incita a las células a producir la “proteína de pico” del coronavirus. Las vacunas no cambian el ADN de las células y, una vez que se crea el pico, las células destruyen la mayor parte del ARNm. Otras inyecciones contra el COVID-19 incluyen vacunas de vectores virales fabricadas por AstraZeneca y Johnson & Johnson, que introducen ADN en las células para hacer que produzcan proteínas de pico. Las células que producen las proteínas de pico, siguiendo instrucciones de vacunas de ARNm o de vectores virales, son atacadas por el sistema inmunológico, por lo que no permanecen por mucho tiempo. Esto es diferente de la terapia génica, cuyo objetivo es cambiar la función celular a largo plazo.
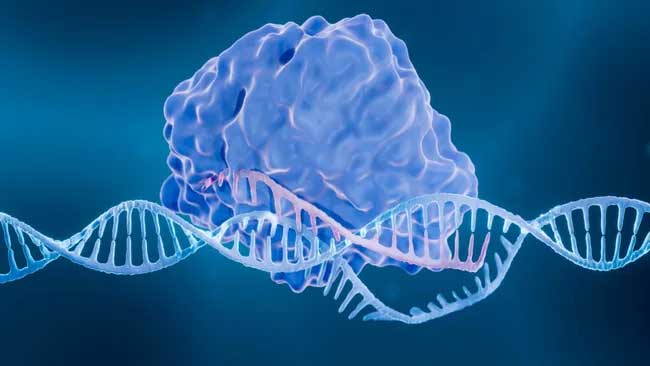
El ADN es una molécula que almacena información genética y los genes son fragmentos de información genética que las células utilizan para producir un producto específico, como una proteína. El ADN se encuentra dentro del núcleo celular, donde se empaqueta en cromosomas, y también dentro de las mitocondrias, los orgánulos “centrales” ubicados fuera del núcleo.
Si bien hay enfermedades mitocondriales que algún día podrían tratarse con terapia génica, actualmente el término “terapia génica” se refiere a tratamientos dirigidos a genes nucleares: los genes de los 23 pares de cromosomas dentro del núcleo.
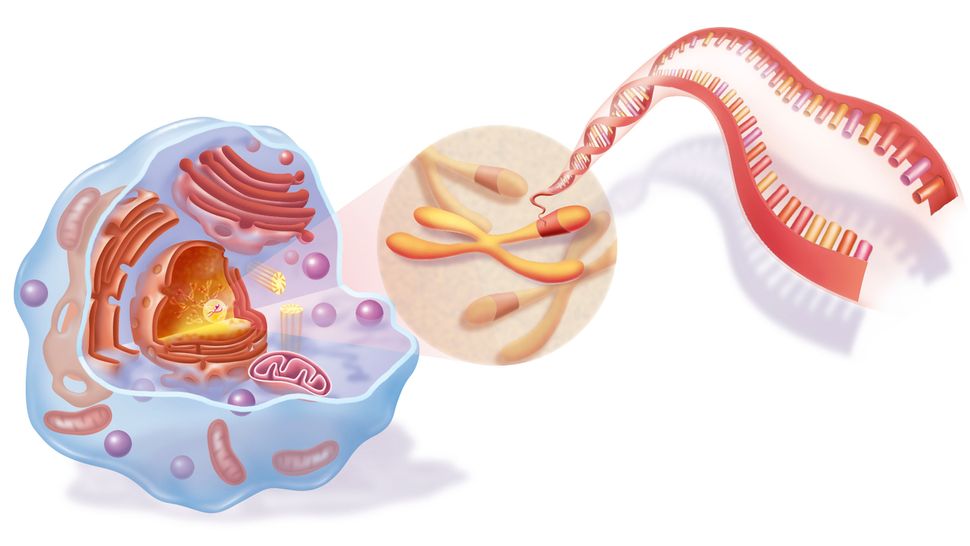
Ilustración del ADN dentro de los cromosomas, que luego se encuentran dentro del núcleo de una célula. BSIP/UIG
Clásicamente, la terapia génica se refiere al proceso de “desactivar” un gen disfuncional o agregar una copia de un gen funcional al núcleo con el objetivo de mejorar la función celular. Actualmente, la terapia génica se dirige a enfermedades que surgen de un problema con un solo gen o como máximo con unos pocos genes, en lugar de aquellas que afectan a muchos genes.
Sin embargo, el campo de la terapia génica se está expandiendo para incluir estrategias que no todas caen en las categorías clásicas de eliminar genes malos o agregar genes buenos. Por ejemplo, los investigadores de Sangamo Therapeutics están desarrollando tratamientos genéticos para las enfermedades de Parkinson, Alzheimer y Huntington que funcionan mejorando o suprimiendo la actividad de genes específicos.
Aunque los tratamientos pueden agregar genes a células del cuerpo, desactivar genes o cambiar la función de los genes de alguna manera, cada terapia génica se dirige a células de tejidos corporales específicos. Por lo tanto, cuando los científicos y médicos hablan de lo que la terapia génica le hace al ADN, no se refieren a todo el ADN del cuerpo, sino sólo a una parte de él.
La terapia génica se puede realizar tanto ex vivo como in vivo.
La terapia génica ex vivo significa que las células se extraen del cuerpo, se procesan y luego se devuelven al cuerpo. Este es un enfoque utilizado para tratar enfermedades genéticas de las células sanguíneas, en el que se puede extraer médula ósea del paciente y las células madre de esa médula ósea se pueden tratar con terapia génica, por ejemplo, para reemplazar un gen que falta o que no funciona correctamente. —Y las células transformadas se pueden inyectar nuevamente al paciente.
La terapia génica in vivo significa que la terapia génica en sí se administra o infunde a una persona. Esto podría ser una inyección directamente en el sitio anatómico donde se necesita la terapia génica (un ejemplo común es la retina), o podría significar una inyección o infusión de la carga genética que se entregará al tejido corporal donde se necesita.
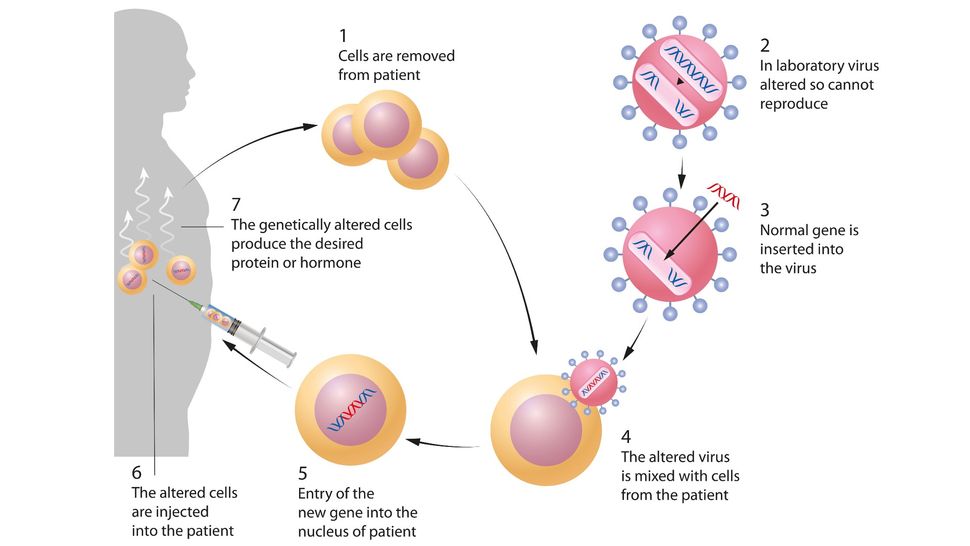
La terapia génica puede implicar la introducción de genes en células y tejidos humanos para tratar una enfermedad. Este diagrama muestra un ejemplo de terapia génica ex vivo. Aldona Grishkeviciene
Tanto en la terapia génica ex vivo como en vivo, la carga genética se empaqueta en un contenedor llamado vector antes de ser entregada a las células o al cuerpo. Uno de esos vectores es el virus adenoasociado (AAV). Se trata de un grupo de virus que existen en la naturaleza, pero cuyos genes normales han sido eliminados y sustituidos por una carga genética, convirtiéndolos en vectores de terapia génica.
El AAV se ha utilizado para administrar terapia génica durante muchos años porque tiene un buen historial de seguridad. Es mucho menos probable que desencadene una respuesta inmunitaria peligrosa que otros virus que se utilizaron como vectores hace décadas, cuando la terapia génica estaba en su infancia. Además, empaquetar cargas genéticas en portadores de AAV permite que la terapia génica inyectada o infundida viaje a tejidos corporales específicos donde es necesaria. Esto se debe a que existen muchos tipos de AAV y ciertos tipos se sienten atraídos por ciertos tejidos u órganos. Entonces, si la carga genética necesita llegar a las células del hígado, por ejemplo, se puede empaquetar en un tipo de AAV al que le gusta ir al hígado.
En los primeros días de la terapia génica, que comenzó en 1989, los investigadores utilizaron retrovirus como vectores. Estos virus entregaron carga genética directamente a los cromosomas nucleares del paciente. Sin embargo, existía la preocupación de que esta integración de nuevo ADN en los cromosomas pudiera provocar cambios que condujeran al cáncer, por lo que inicialmente se abandonó esta estrategia. (Más recientemente, los científicos han utilizado con éxito retrovirus en terapia genética experimental sin causar cáncer; por ejemplo, la terapia basada en retrovirus se ha utilizado para tratar a bebés con la “enfermedad del niño burbuja”).
Alejándose de los retrovirus, los investigadores recurrieron a los adenovirus, que ofrecían la ventaja de entregar la carga genética en forma de episoma, un fragmento de ADN que funciona como un gen dentro del núcleo pero sigue siendo una entidad separada de los cromosomas. El riesgo de cáncer era extremadamente bajo con esta innovación, pero los vectores adenovirales resultaron estimular el sistema inmunológico de maneras muy poderosas. En 1999, una reacción inmune a la terapia genética que utilizaba un adenovirus provocó la muerte de Jesse Gelsinger, de 18 años, quien se ofreció como voluntario para participar en un ensayo clínico.

Los investigadores de terapia génica abandonaron el uso de retrovirus y pasaron a los adenovirus. Seksan Mongkhon Khamsao
La muerte de Gelsinger conmocionó a la comunidad de terapia genética, paralizando el campo durante varios años, pero las terapias genéticas modernas basadas en AAV que han surgido a lo largo de los años no son peligrosas. Sin embargo, tienden a ser costosos y las tasas de éxito varían, por lo que generalmente se utilizan como último recurso para un número creciente de enfermedades genéticas.
La terapia génica puede tratar algunas enfermedades de la sangre como la hemofilia A, la hemofilia B, la anemia falciforme y, a partir de 2022, la beta talasemia. Lo que estas enfermedades tienen en común es que el problema se reduce a un solo gen. Esto ha hecho que la beta talasemia y la anemia de células falciformes estén fácilmente disponibles para la terapia génica ex vivo, que implica eliminar y modificar células madre de la médula ósea, mientras que la hemofilia A y la hemofilia B se tratan con terapia génica in vivo dirigida a las células del hígado. Sin embargo, existen otros tratamientos para estos trastornos sanguíneos, por lo que la terapia génica es más bien un último recurso.
Numerosos trastornos por deficiencia de enzimas también se deben a un gen defectuoso que debe ser reemplazado. La adrenoleucodistrofia cerebral, que provoca una acumulación de ácidos grasos en el cerebro, es uno de esos trastornos que puede tratarse con terapia génica, según el Boston Children’s Hospital. La terapia de células T con CAR, que está aprobada para algunos cánceres, implica eliminar y modificar las células inmunitarias del paciente y se conoce como “terapia genética basada en células”.
La terapia génica también ha demostrado ser útil en el tratamiento de enfermedades hereditarias de la retina en las que otros tratamientos han fracasado. Otro grupo de objetivos de la terapia génica son las enfermedades del sistema nervioso.
Por ejemplo, se está desarrollando una terapia genética para tratar un par de enfermedades genéticas llamadas enfermedad de Tay-Sachs y enfermedad de Sandhoff. Ambas condiciones ocurren porque los orgánulos llamados lisosomas se llenan de moléculas parecidas a grasas llamadas gangliósidos. Las consecuencias de estas enfermedades incluyen retrasos en el desarrollo, pérdida de habilidades previamente adquiridas, rigidez, ceguera, debilidad y falta de coordinación con posible parálisis. Los niños que nacen con la enfermedad de Tay-Sachs y la enfermedad de Sandhoff generalmente no sobreviven más allá de los 2 a 5 años de edad.
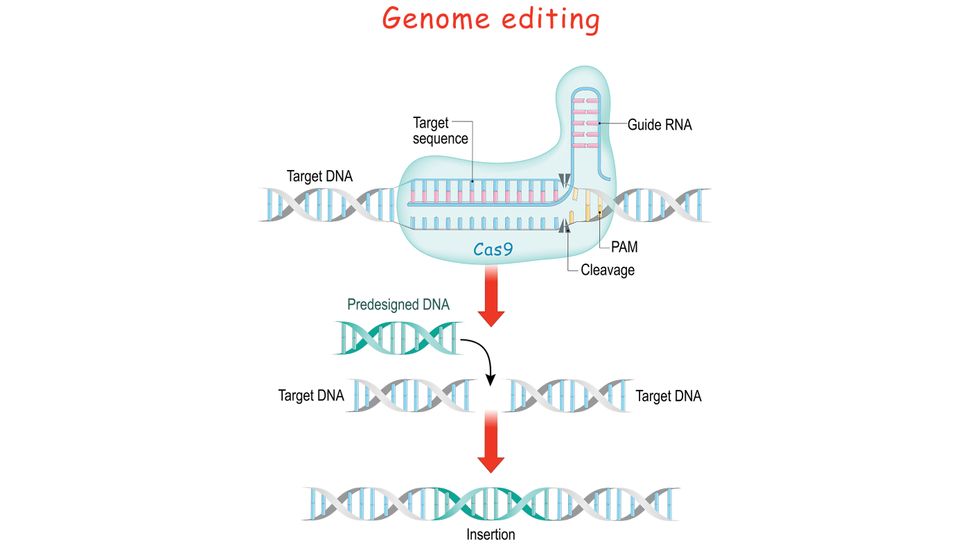
La edición de genes CRISPR es un método poderoso para modificar el ADN que algún día podría usarse en terapia génica. Aquí hay una descripción simplificada de cómo funciona la edición de genes CRISPR. ttsz
“No existían pruebas prenatales o neonatales racionales para el síndrome de Tay-Sachs y el síndrome de Sandhoff porque no había ningún tratamiento disponible”, dijo el Dr. Jagdeep Walia, genetista clínico y jefe de genética médica del Departamento de Pediatría y Centro de Ciencias de la Salud de Kingston y Queen’s University en Ontario, Canadá. Walia está desarrollando una terapia génica destinada a sustituir el gen Hex A, una enzima deficiente en estos niños. Hasta ahora, el tratamiento ha demostrado buena eficacia y seguridad en modelos animales, pero aún debe probarse en humanos.
El futuro parece prometedor en lo que respecta a la terapia génica en general, gracias a los nuevos avances tecnológicos, incluida la edición de genes CRISPR. Este es un método extremadamente poderoso para cortar partes de moléculas de ADN e incluso insertar partes nuevas. CRISPR no es el primer método que los científicos utilizan para editar el ADN, pero es mucho más versátil que otros métodos. Todavía no está preparado para la manipulación cromosómica in vivo, pero está evolucionando exponencialmente.
Quizás aún más cerca del horizonte esté la perspectiva de introducir más información genética en las células. Una de las grandes desventajas del vector AAV es que cada partícula de virus sólo puede transportar una pequeña cantidad de ADN, pero investigaciones recientes han demostrado que otro tipo de virus, llamado citomegalovirus, puede adaptarse para transportar terapia génica con información mucho más útil que la VAA. Esto no sólo podría algún día expandir la terapia genética a más enfermedades que requieran más genes de los que el AAV puede transportar, sino que también podría permitir que se administre más de un gen en una sola terapia.