La MHRA ha aprobado Casgevy para el tratamiento de la anemia de células falciformes (SCD) y la beta talasemia dependiente de transfusiones. Se trata de trastornos genéticos de por vida causados por mutaciones en los genes que codifican la hemoglobina, una proteína que necesitan los glóbulos rojos para transportar oxígeno por todo el cuerpo. CRISPR podría tratar una forma común de ceguera hereditaria. El Premio Nobel de Química 2020 fue para dos mujeres que desarrollaron una herramienta de edición genética llamada CRISPR-Cas9, que corta el ADN como si fuera una tijera molecular.
Los científicos presentaron CRISPR al mundo como una herramienta de edición de genes en el verano de 2012, cuando artículos históricos de dos grupos independientes demostraron cómo el sistema podría usarse para cortar ADN. Ahora estamos viendo que CRISPR se utiliza en tratamientos médicos innovadores.
Antes de estos artículos trascendentales, otros investigadores comenzaron a desentrañar cómo funcionaba CRISPR dentro de los microbios. Aunque CRISPR es más conocido como herramienta de edición de genes, se descubrió por primera vez en bacterias y los científicos se dieron cuenta de que actúa como una especie de sistema inmunológico: una defensa contra los virus. En este sistema inmunológico, la bacteria tiene un banco de memoria lleno de material genético del virus. La bacteria retendrá este material tras ser atacada por el virus para protegerse de futuras invasiones.
Este banco de memoria está emparejado con pequeñas tijeras moleculares llamadas proteínas Cas, que cortan el ADN, y una molécula que guía las tijeras hacia su objetivo. En las bacterias, este objetivo es un invasor viral. Šikšnis y sus colegas demostraron que los científicos pueden utilizar estas tijeras a su favor, apuntando a cualquier ADN que quieran editar. Lo demostraron específicamente utilizando la proteína Cas9 como ejemplo.
Junto con Jennifer Doudna y Emmanuelle Charpentier, autoras de otro artículo innovador sobre CRISPR publicado en 2012, Sikshnis recibió el Premio Kavli de Nanociencia 2018 por su invención de CRISPR-Cas9, una “nanoherramienta de precisión para la edición de ADN”. Actualmente, él y su equipo están explorando la diversidad de sistemas CRISPR que se encuentran en la naturaleza para ver cuáles podrían ser útiles para diseñar genomas.
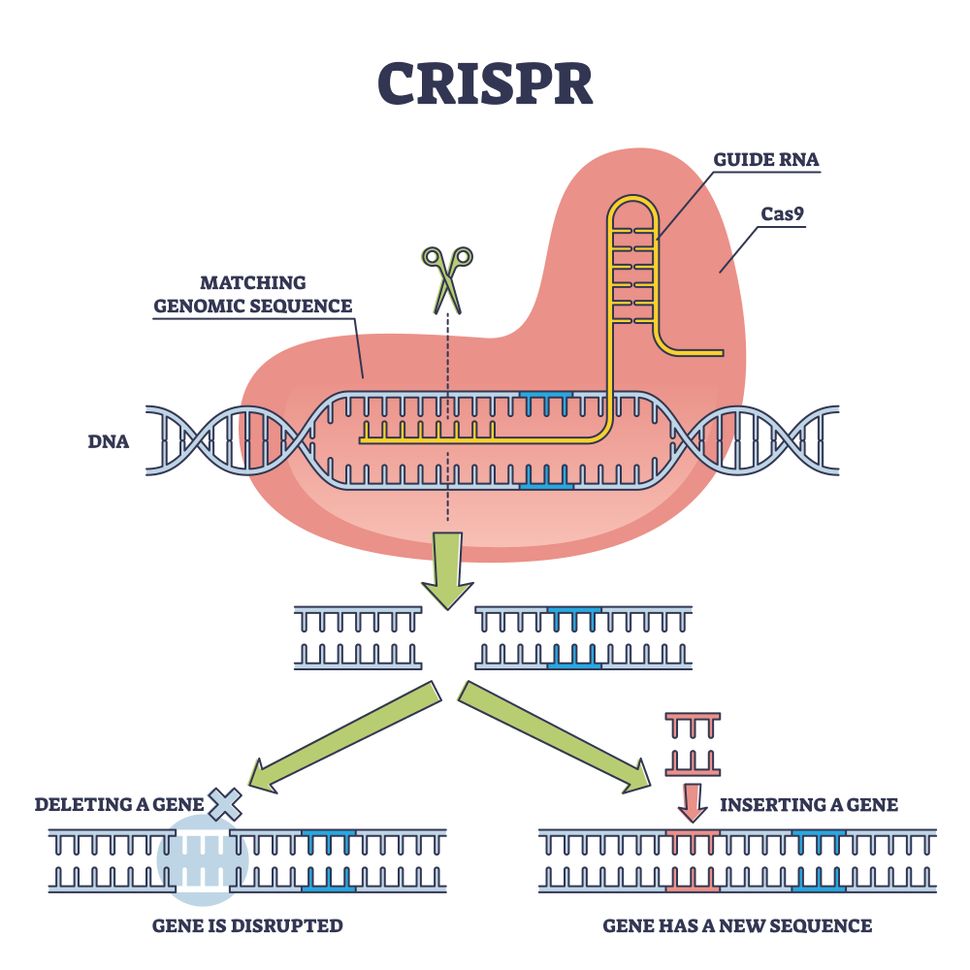
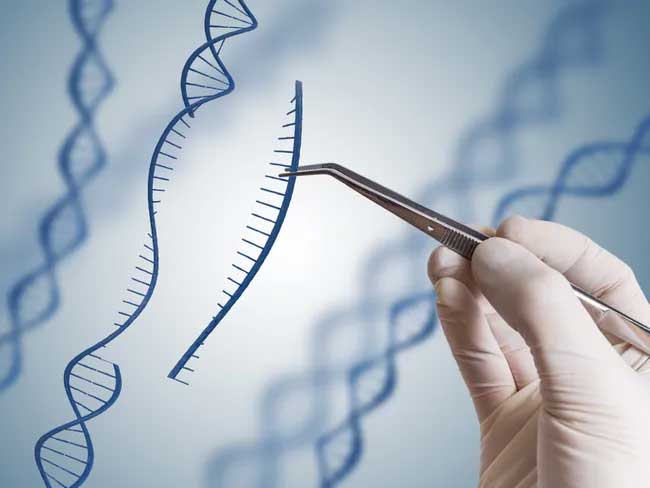
El sistema CRISPR-Cas9 utiliza Cas9 como tijera molecular y una molécula de ARN como guía para las tijeras.
Un artículo de 2012 demostró que es posible reprogramar la proteína Cas9 y dirigirla a cualquier secuencia del genoma. Es realmente un sistema realmente versátil que puede usarse para la edición del genoma en una variedad de organismos modelo.
Este tratamiento tiene varias limitaciones porque en este caso el tratamiento ocurre ex vivo. Esto significa que las células a tratar se eliminan del cuerpo del paciente y luego se utiliza una herramienta Cas9 para corregir la mutación o, esencialmente, desencadenar la producción de hemoglobina fetal. Y luego estas células diseñadas tienen que ser devueltas al cuerpo del paciente. Y, por supuesto, se trata de un procedimiento largo y complejo.
Por supuesto, sería fantástico si los tratamientos CRISPR pudieran realizarse directamente en el cuerpo humano; a esto lo llamamos in vivo. Pero en realidad, para hacer esto, hay varios desafíos que deben superarse: primero, debemos introducir esta herramienta CRISPR en tejidos u órganos específicos del cuerpo humano. Y, por supuesto, hay muchas formas de ofrecer herramientas CRISPR, pero desde la COVID, las vacunas de ARNm han sido aprobadas como una opción terapéutica para el tratamiento y la prevención de la COVID. Y ahora, el ARNm en combinación con nanopartículas lipídicas se ha convertido en uno de los métodos clave que pueden administrar Cas9 a diversas células y tejidos del cuerpo humano.
También se están explorando otros sistemas de administración, incluidas partículas similares a virus y virus adenoasociados. Por lo tanto, los AAV también se utilizan como vehículos de entrega y están aprobados como vehículos de entrega seguros en el cuerpo humano, pero con los AAV, por ejemplo, existe una limitación de carga de empaque y es necesario encontrar herramientas de edición de genes más pequeñas que puedan empaquetarse en uno. Partícula AAV.

Virginijus Siksnis estudia la diversidad de sistemas CRISPR que se encuentran en la naturaleza. Universidad de Vilna
En primer lugar, los investigadores estudian secuencias de ADN microbiano que están presentes en enormes bases de datos, donde se pueden encontrar nuevos sistemas CRISPR. Luego se hacen esfuerzos para expresarlos en diferentes bacterias, aislarlos, caracterizarlos y luego transferirlos a células humanas para ver si pueden usarse como nuevas herramientas para la modificación del genoma.
Estaba claro desde el principio que las enfermedades genéticas causadas por una sola mutación, como la anemia falciforme, serían el primer objetivo. Esto parecía fácilmente alcanzable porque sólo era necesario corregir una mutación en el genoma. Parte del crédito por este tratamiento de células falciformes basado en Cas9 debería recaer en las personas que han estado estudiando la enfermedad de células falciformes durante décadas. Proporcionaron información sobre los mecanismos de la enfermedad implicados en el tratamiento.
CRISPR-Cas9 es un tipo de tecnología universal o multifuncional porque puede usarse para crear cualquier organismo vivo. Simplemente estás intentando crear ADN, y el ADN es el modelo de todo organismo vivo. Entonces, en lugar de editar genes en células humanas, también podría pensar en editar una población de bacterias, por ejemplo, las que se encuentran en el intestino humano. Y estas poblaciones bacterianas se pueden crear.
Las tecnologías CRISPR también se pueden utilizar como agentes antivirales. Actualmente, el problema con los antibióticos es bastante claro: probablemente estemos perdiendo la batalla contra las bacterias al usarlos. Siempre se necesitan nuevos antibióticos y son realmente difíciles de encontrar, difíciles y caros. Por ello, se están desarrollando tecnologías alternativas, como la terapia viral o los sistemas antibacterianos CRISPR.
CRISPR se utilizó hace unos años en China para crear embriones humanos, por lo que esta es una línea que los científicos en realidad no están dispuestos a cruzar porque podría ser realmente peligroso.
Exa-cel, también conocido por la marca Casgevy, recibió su primera aprobación regulatoria el 16 de noviembre de 2023 de la Agencia Reguladora de Medicamentos y Productos Sanitarios del Reino Unido (MHRA) para el tratamiento de dos enfermedades sanguíneas debilitantes: la anemia falciforme y la dependiente de transfusiones enfermedad de células beta. La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó posteriormente esta terapia como tratamiento para ambas enfermedades.
Se ha aprobado el primer tratamiento del mundo que utiliza la tecnología de edición de genes CRISPR. Los reguladores de medicamentos han aprobado una terapia CRISPR llamada Casgevy para tratar trastornos sanguíneos hereditarios.
La histórica decisión de los reguladores de aprobar Casgevy podría señalar el comienzo de una nueva era de la terapia génica. Sin embargo, quedan dudas sobre la disponibilidad del tratamiento y su seguridad a largo plazo.
La MHRA ha aprobado Casgevy para el tratamiento de la anemia de células falciformes (SCD) y la beta talasemia dependiente de transfusiones. Se trata de trastornos genéticos de por vida causados por mutaciones en los genes que codifican la hemoglobina, una proteína que necesitan los glóbulos rojos para transportar oxígeno por todo el cuerpo.
Se estima que más de 100.000 personas en los Estados Unidos tienen ECF, pero la tasa es más alta en algunas poblaciones que en otras. Por ejemplo, 1 de cada 365 niños negros nace con ECF. La enfermedad cambia la forma de los glóbulos rojos de una persona para que tengan forma de C en lugar de redondos. Las células falciformes mueren rápidamente y también se pegan entre sí, bloqueando los vasos sanguíneos. Como resultado, los pacientes desarrollan anemia y a menudo experimentan ataques de dolor intenso, llamados crisis de dolor.
La beta talasemia afecta aproximadamente a 1 de cada 100.000 personas en todo el mundo y afecta desproporcionadamente a personas de origen mediterráneo, asiático, africano y de Oriente Medio. Los pacientes con beta talasemia no producen suficiente hemoglobina, lo que puede provocar una anemia grave, mientras que la anemia falciforme se produce debido a la falta de glóbulos rojos sanos. “Dependiente de transfusiones” significa que la enfermedad es tan grave que los pacientes necesitan transfusiones periódicas de glóbulos rojos durante toda su vida.
Casgevy se basa en una revolucionaria tecnología de edición de genes llamada CRISPR, que se desarrolló por primera vez en 2012. El sistema CRISPR corta genes del ADN utilizando la enzima Cas9. Estas “tijeras moleculares” se dirigen al ADN objetivo mediante una molécula de ARN. La tecnología se adaptó a partir de un mecanismo de defensa natural que las bacterias y otros organismos simples llamados arqueas utilizan contra los virus.
Casgevy se dirige al gen BCL11A. El gen codifica una proteína que normalmente regula el cambio de la versión fetal de la hemoglobina a la versión adulta poco después del nacimiento. Sin embargo, en pacientes con ECF y beta talasemia, la hemoglobina adulta es defectuosa.
El objetivo de Casgevy es desactivar BCL11A y así permitir que el cuerpo siga produciendo hemoglobina fetal, ya que la versión para adultos no funciona. Para ello, se extraen células madre hematopoyéticas de la médula ósea del paciente y se edita el gen BCL11A utilizando Casgevy en el laboratorio. Las células modificadas con hemoglobina funcional se vuelven a infundir en el cuerpo del paciente. Antes de la infusión, el paciente debe tomar un fármaco de quimioterapia llamado busulfano para eliminar las células no editadas que aún se encuentran en la médula ósea, informa STAT News.
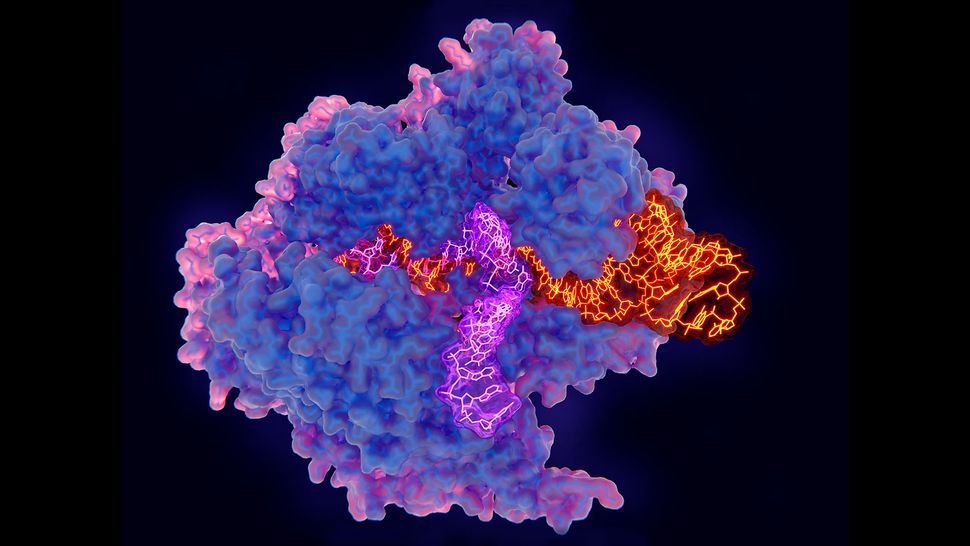
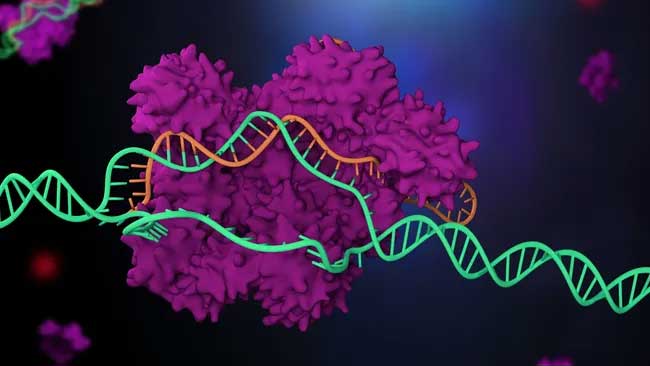
Esta ilustración de CRISPR en acción muestra Cas9 (azul y rosa) adherido al ADN (púrpura) junto a una molécula de ARN guía (naranja). JUAN GAERTNER/BIBLIOTECA DE FOTOS DE LA CIENCIA
Este proceso de adaptación a células nuevas y editadas es largo. “Es posible que los pacientes necesiten pasar al menos un mes en el hospital mientras las células tratadas se asientan en la médula ósea y comienzan a producir glóbulos rojos con una forma estable de hemoglobina”, dijo la MHRA en un comunicado.
En dos ensayos clínicos de última etapa, Casgevy restableció la producción de hemoglobina en la mayoría de los pacientes con ECF y beta talasemia y mejoró sus síntomas. Veintiocho de 29 pacientes con ECF no experimentaron ninguna crisis de dolor grave durante al menos un año después del tratamiento con Casgevy. De manera similar, 39 de 42 pacientes con beta talasemia no necesitaron transfusiones de glóbulos rojos durante el mismo período después del tratamiento. Los tres pacientes restantes requirieron transfusiones con una frecuencia más del 70% menor.
No se observaron problemas graves de seguridad de los medicamentos en ninguno de los dos ensayos clínicos de última etapa de Casgevy, aunque se informaron algunos efectos secundarios temporales, como fiebre y fatiga. Ambos ensayos están en curso y la seguridad a largo plazo de Casgevy continúa siendo monitoreada por reguladores como la MHRA y la FDA, así como por los fabricantes de terapias Vertex Pharmaceuticals y CRISPR Therapeutics.
Sin embargo, todavía existen algunas preocupaciones sobre la seguridad general de las terapias basadas en CRISPR. Es decir, existen preocupaciones sobre los efectos “fuera del objetivo”, que ocurren cuando Cas9 actúa en otras partes del genoma que no estaban destinadas a cambiar, causando efectos secundarios no deseados.
“Es bien sabido que CRISPR puede conducir a modificaciones genéticas espurias con consecuencias desconocidas para las células tratadas”, dijo David Rueda, jefe del departamento de biofísica molecular y celular del Imperial College de Londres, al Science Media Centre del Reino Unido. “Necesitamos ver todos los datos de secuenciación del genoma de estas células antes de poder sacar conclusiones”, dijo. Esto implicará examinar todo el ADN de las células editadas por Kasgewi para ver si hay algún efecto fuera del objetivo.
En noviembre de 2023, el Reino Unido aprobó Casgevy para personas mayores de 12 años con anemia falciforme o beta talasemia dependiente de transfusiones. En diciembre, la FDA aprobó el tratamiento para personas de 12 años o más con anemia de células falciformes, y en enero de 2024, la agencia aprobó Casgevy para personas con beta talasemia dependiente de transfusiones en la misma categoría de edad.
Actualmente, el tratamiento está siendo revisado por la Agencia Europea de Medicamentos de la Unión Europea y la Administración de Alimentos y Medicamentos de Arabia Saudita, por lo que otros países pronto podrían aprobar Casgevy, según Vertex.
No está claro cuándo estará disponible Casgevy, pero su alcance dependerá en gran medida de su costo. La terapia genética puede costar millones de dólares y parece que Casgevy no será una excepción. Esto puede dejarlo fuera del alcance de muchas personas que lo necesitan.
“El problema es que estos tratamientos serán muy caros, por lo que la clave es que estén más disponibles en todo el mundo”, dijo Kay Davies, profesora de anatomía de la Universidad de Oxford, al British Science Media Center.
Un portavoz de Vertex dijo a Nature que la compañía aún no ha fijado un precio para Casgevy en el Reino Unido, pero está “trabajando con las autoridades sanitarias para garantizar el reembolso y el acceso al medicamento para los pacientes elegibles lo antes posible”.
Intellia Therapeutics está desarrollando terapias CRISPR para tratar enfermedades hereditarias dentro del cuerpo, informa STAT News. Además, se está probando una versión modificada de CRISPR llamada “edición de bases” que puede apuntar a bloques de construcción de ADN individuales como una forma de tratar enfermedades. Por ejemplo, Verve Therapeutics está probando un tratamiento experimental para enfermedades cardíacas. Otro nuevo y prometedor tipo de terapia, llamado “edición de bases”, involucra CRISPR pero también “incluye enzimas adicionales e instrucciones genéticas para insertar, eliminar o reescribir segmentos cortos de ADN”, informa STAT News.
CRISPR podría tratar una forma común de ceguera hereditaria, sugiere la evidencia preliminar. En un pequeño estudio, algunas personas con pérdida de visión hereditaria vieron una mejor visión después del tratamiento con CRISPR.
Los primeros ensayos clínicos sugieren que la terapia CRISPR inyectada directamente en el ojo puede resultar prometedora en el tratamiento de la forma más común de pérdida de visión hereditaria en los niños.
Esta forma de pérdida de visión, llamada amaurosis congénita de Leber (LCA), a menudo aparece al nacer y es resultado de una disfunción o muerte de células sensibles a la luz llamadas fotorreceptores en la retina, en la parte posterior del ojo. Estos problemas surgen de mutaciones en cualquiera de al menos 20 genes.
Algunas de las causas más comunes de LCA son mutaciones en el gen que codifica la proteína centrosomal 290 (CEP290). Más de las tres cuartas partes de las personas con la enfermedad portan una mutación específica que afecta a CEP290, que es fundamental para el correcto funcionamiento de los fotorreceptores.
Actualmente no existe cura para el LCA, pero ahora hay evidencia de que la famosa herramienta de edición de genes CRISPR puede usarse de manera segura para mejorar la visión de algunas personas con esta afección. Los resultados de la fase inicial del estudio se publicaron en The New England Journal of Medicine.
El ensayo también es notable porque incluyó a la primera persona que recibió un tratamiento basado en CRISPR directamente en el cuerpo. En comparación, la primera terapia CRISPR aprobada implica tomar células del cuerpo, editarlas en el laboratorio y luego devolvérselas al paciente.
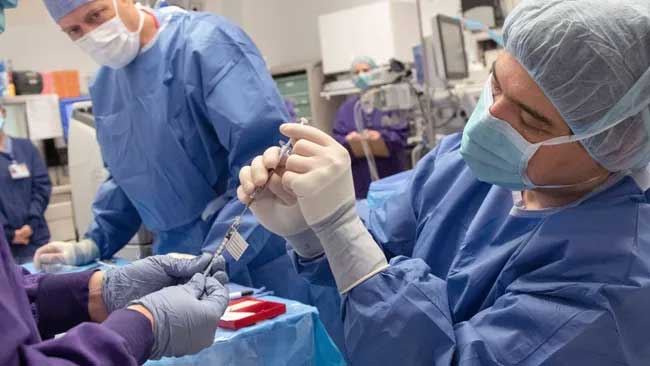
Aquí, los cirujanos del Casey Eye Institute de OHSU realizan la edición de genes CRISPR en el cuerpo como parte de un ensayo clínico reciente. OHSU/Kristyna Wentz-Graff
En el estudio participaron 14 personas: 12 adultos y dos niños. Todos ellos tenían una mutación específica en el gen CEP290, que afecta a la mayoría de los pacientes con LCA. Los participantes recibieron una inyección de un medicamento CRISPR llamado EDIT-101 en el ojo con la pérdida de visión más significativa. El otro ojo sirvió de comparación.
EDIT-101 contiene pequeñas guías que guían pares de “tijeras moleculares” (llamadas enzimas Cas9) hasta el gen mutante CEP290. Las tijeras cortaron la parte defectuosa del gen, restableciendo así su función.
El equipo utilizó una estrategia basada en CRISPR porque CEP290 es un gen grande, lo que lo convierte en un objetivo difícil para la terapia génica tradicional. Algunas terapias genéticas utilizan virus modificados para administrar genes funcionales a las células para reemplazar genes defectuosos, pero el gen CEP290 es demasiado grande para caber en dicho sistema de administración.
Después de este tratamiento, todos los participantes se sometieron a pruebas de visión, que se llevaron a cabo cada tres meses durante un año, seguidas de un seguimiento menos frecuente durante dos años. Al final del período de prueba, 11 de los 14 voluntarios mostraron mejoras mensurables en al menos una prueba de visión, mientras que seis experimentaron mejoras en dos o más pruebas. Un participante del ensayo compartió que podía encontrar su teléfono si lo perdía y podía ver las pequeñas luces de su máquina de café, algo que no podía hacer antes del tratamiento.
Aquellos que no mostraron mejoras mensurables tendían a estar en una etapa posterior de la enfermedad, en la que sus células mostraban altos niveles de disfunción al inicio del estudio, anotaron los participantes del estudio. Ninguno de los participantes experimentó ningún efecto secundario adverso del tratamiento.
Aunque EDIT-101 puede tratar células presentes en la retina, no puede revertir la pérdida de células que ya han muerto. Esto significa que los participantes pueden experimentar cierta mejora en la visión, pero ésta sigue siendo reducida.
El siguiente paso será probar la terapia en más pacientes. El equipo espera especialmente probar el fármaco en pacientes más jóvenes, que esperamos puedan obtener resultados aún mejores.
El Premio Nobel de Química 2020 fue para dos mujeres que desarrollaron una herramienta de edición genética llamada CRISPR-Cas9, que corta el ADN como si fuera una tijera molecular.
La tecnología “no sólo ha revolucionado la ciencia básica, sino que también ha dado lugar a cultivos innovadores y conducirá a nuevos tratamientos innovadores”, dijo en un comunicado Klaas Gustafsson, presidente del Comité Nobel de Química. Con la capacidad de cortar hábilmente secuencias de ADN específicas del genoma, los científicos pueden identificar la función genética; Estos descubrimientos no sólo contribuyen a nuestra comprensión básica de cómo funcionan estos genes, sino que también pueden tener aplicaciones prácticas, como el cultivo de cultivos resistentes a las sequías y las plagas y el desarrollo de tratamientos para el cáncer y las enfermedades genéticas. El sistema genético de cortar y pegar también se está utilizando en nuevas pruebas de diagnóstico de COVID-19.
El Premio Nobel por su desarrollo de la edición del genoma fue para Emmanuelle Charpentier, directora de la unidad de investigación de patógenos de la Sociedad Max Planck, y Jennifer Doudna, profesora de bioquímica, biofísica y biología estructural de la Universidad de California, Berkeley. Según la revista Science, este es el primer Premio Nobel científico otorgado a un equipo exclusivamente femenino.
El desarrollo de CRISPR-Cas9 comenzó por casualidad cuando Charpentier estaba estudiando la bacteria Streptococcus pyogenes, que causa una variedad de enfermedades desde amigdalitis hasta sepsis, según un comunicado del comité del Nobel. Charpentier descubrió que la bacteria contiene una molécula llamada tracrRNA que protege a S. pyogenes de la infección por virus, según un informe de 2011 en la revista Nature.
Resulta que el ARNtracr es sólo un componente de un mecanismo de defensa más amplio conocido como sistema CRISPR/Cas, que las bacterias utilizan para cortar y degradar el ADN de los virus que intentan infectarlas. Tras un ataque viral, las bacterias incorporan parte del ADN viral a su propio genoma; Estos despojos de batalla se alinean a lo largo del genoma, aparecen repetidamente y se conocen como “grupos de repeticiones palindrómicas cortas regularmente intercaladas”, abreviado como CRISPR. Se cree que estos genes archivados ayudan a las bacterias a reconocer virus y defenderse de futuros ataques.
Pero para cortar primero el ADN viral, las bacterias utilizan proteínas “asociadas a CRISPR” llamadas proteínas Cas, guiadas por ARNtracr y otras moléculas.
Después del descubrimiento del ARNtracr, Charpentier comenzó a colaborar con Doudna y los dos recrearon las tijeras genéticas de las bacterias en un tubo de ensayo. En su trabajo fundamental, publicado en 2012 en la revista Science, simplificaron el sistema y lo convirtieron en una práctica herramienta de edición de genes capaz de seleccionar y cortar secuencias de ADN específicas del genoma. Desde entonces, la herramienta se ha perfeccionado y utilizado para una amplia gama de aplicaciones, incluido el reciente desarrollo de pruebas de diagnóstico para COVID-19, informa la BBC.
“Este descubrimiento, derivado originalmente del mecanismo de defensa natural de las bacterias contra los virus, tendrá innumerables aplicaciones en el tratamiento y cura de enfermedades genéticas y la lucha contra el cáncer, así como impacto en la agricultura y otros campos”, afirmó Luis Echegoyen, presidente. dijo en un comunicado la Sociedad Química Estadounidense. “El futuro de esta tecnología es realmente brillante y prometedor”.
Algunos científicos esperaban que el bioquímico Feng Zhang del Broad Institute compartiera el Premio Nobel con Charpentier y Doudna porque, poco después de su descubrimiento, demostró que CRISPR también funciona en células de mamíferos, informa la revista Science. Basado en el trabajo de Zhang, el Instituto Broad recibió la primera patente para utilizar la tecnología de edición de genes CRISPR en eucariotas (células complejas con núcleos para almacenar ADN), pero los institutos Charpentier y Doudna continúan luchando por sus propias patentes, según The Scientist.