La superbactérie Clostridioides difficile, ou C. diff, peut provoquer de dangereuses infections intestinales. Les options de traitement sont limitées et les patients subissent souvent une réinfection, qui peut être mortelle. De nouvelles recherches montrent désormais que cette bactérie dangereuse peut rapidement développer une résistance aux antibiotiques, même si cette résistance a un coût pour la superbactérie elle-même. Les chercheurs ont identifié deux mécanismes distincts de résistance aux médicaments chez C. difficile.
Les toxines produites par les souches de Clostridioides difficile dans le tractus gastro-intestinal provoquent une colite pseudomembraneuse, généralement après l’utilisation d’antibiotiques. Les symptômes comprennent une diarrhée, parfois sanglante, évoluant rarement vers un mégacôlon toxique, une perforation du côlon, une septicémie et un abdomen aigu.
Selon les auteurs de l’étude, les résultats soulignent la nécessité d’une surveillance attentive de la résistance bactérienne aux antibiotiques, notamment dans les hôpitaux.
Pour la plupart des gens, les bactéries bénéfiques vivant dans l’intestin le protègent des infections. Lorsque ces bactéries meurent, par exemple à la suite d’un traitement antibiotique pour une infection non liée, le côlon devient vulnérable et c’est à ce moment-là que C. difficile l’attaque. Les personnes qui prennent ou ont récemment pris des antibiotiques sont 10 fois plus susceptibles d’être infectées par C. difficile que celles qui n’en ont pas pris. D’autres facteurs de risque incluent le fait d’être hospitalisé ou dans une maison de retraite, d’avoir un système immunitaire affaibli ou d’être très jeune ou très vieux.
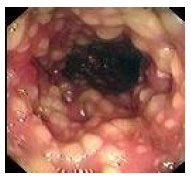
Colite pseudomembraneuse
Malheureusement, seuls trois antibiotiques sont disponibles pour traiter les infections à C. difficile. La vancomycine est le médicament de choix pour la plupart des patients, mais chez environ un tiers des patients, l’infection réapparaît dans le mois suivant la fin du traitement. Une raison possible à cela, suggèrent les auteurs de l’étude, est que C. difficile évolue pour résister à la vancomycine.
“Nous ne savons pas si des souches résistantes circulent et provoquent des infections humaines, car les laboratoires hospitaliers ne testent pas la résistance à la vancomycine”, a déclaré à Live Science l’auteur de l’étude Jessica Buddle, doctorante à l’Université de Sheffield au Royaume-Uni. «Il n’y a eu que quelques cas de résistance dans le monde. Cependant, étant donné le manque de tests, ce n’est probablement pas tout.»
Pour savoir si les bactéries pourraient développer une résistance à la vancomycine, les chercheurs ont modifié génétiquement deux populations de C. difficile: une avec un taux de mutation normal et une qui a évolué plus rapidement. Pour la nouvelle étude, publiée le 15 août dans la revue PLOS Biology, ils ont cultivé cinq souches de chaque population en présence de concentrations croissantes de vancomycine.
En quatre jours, neuf des dix souches ont développé une résistance à la vancomycine; à la fin de l’expérience de 60 jours, les 10 souches étaient capables de se développer avec 32 fois la quantité de vancomycine généralement utilisée pour traiter les infections à C. difficile.
Bien que la bactérie ait utilisé plusieurs mutations génétiques différentes pour échapper à la vancomycine, toutes les souches résistantes avaient un point commun: elles ne pouvaient pas se développer aussi vite que C. difficile, qui n’a pas développé de résistance à la vancomycine. De plus, plusieurs souches étaient plus petites ou avaient du mal à produire des spores, que la bactérie utilise pour survivre et se propager dans l’environnement.
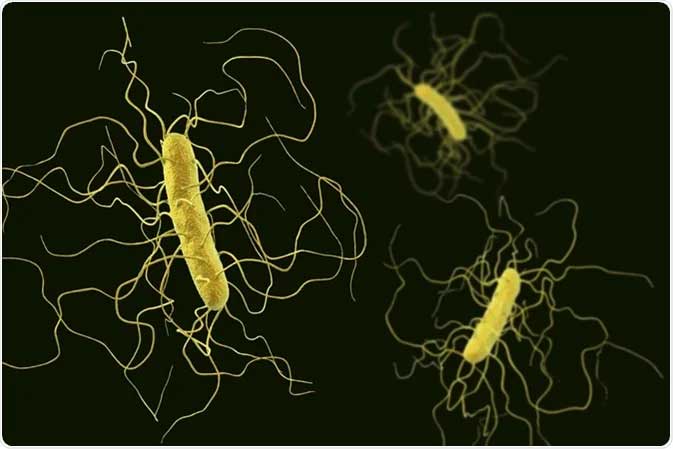
Clostridium difficile
“Dans cette étude, la résistance développée par C. difficile à la vancomycine est vouée à l’échec car elle semble également réduire la capacité de la bactérie à survivre par d’autres moyens”, a déclaré le Dr Paul Feuerstadt, gastro-entérologue et professeur clinicien de médecine, à Live Science. dans un e-mail à la Yale School of Medicine dans le Connecticut. C’est peut-être la raison pour laquelle une résistance élevée à la vancomycine n’est pas aussi courante chez C. difficile que chez certaines autres bactéries, a-t-il ajouté.
Cependant, comprendre et prévenir la résistance aux antibiotiques est essentiel pour garantir la traitabilité des infections à C. difficile.
Savoir comment C. difficile résiste aux antibiotiques permet aux scientifiques de développer de nouveaux traitements auxquels il est plus difficile de résister, a déclaré Feuerstadt, qui n’a pas participé à l’étude. L’élimination rapide et efficace des infections empêche non seulement les bactéries de devenir résistantes, mais signifie également qu’elles ne peuvent pas survivre assez longtemps pour développer une croissance plus rapide ou une meilleure transmission.
“Identifier le problème de résistance signifie que nous ferons les bons choix dans les futures recommandations de traitement”, a déclaré Buddle. «Si nous utilisons le bon médicament pour traiter l’infection et terminons le traitement complet comme prescrit, nous augmentons les chances de réussir à éliminer l’infection et réduisons le risque de résistance. Nous devons considérer les antibiotiques comme une ressource précieuse – et chacun doit faire sa part.»
Parallèlement, les bactéries résistantes aux antibiotiques pourraient tuer plus de 39 millions de personnes au cours des 25 prochaines années, selon une étude réalisée par une équipe internationale de scientifiques et publiée dans un article de la revue médicale Lancet.
«Nous estimons que d’ici 2050, il y aura 1,91 million de décès liés à la RAM et 8,22 millions de décès liés à la RAM dans le monde chaque année. Au cumul, de 2025 à 2050, notre scénario de référence prévoit 39,1 millions de décès attribuables à la RAM et 169 millions de décès attribuables à la RAM», indique l’article.
Les scientifiques prédisent le plus grand nombre de décès en Asie du Sud et de l’Est, ainsi qu’en Océanie et en Afrique subsaharienne.
Les agents pathogènes bactériens auxquels les antibiotiques ne répondent pas sont appelés résistants ou superbactéries. Selon les statistiques de l’OMS, les infections associées constituent la troisième cause de décès dans le monde après les maladies cardiaques et les accidents vasculaires cérébraux. En 2019, 4,95 millions de personnes en sont mortes. Le plus préoccupant est Staphylococcus aureus, qui est résistant à la méthicilline et à d’autres antibiotiques.
Clostridia difficile (lat. Clostridioides difficile, nom traditionnel Clostridium difficile, synonyme Peptoclostridium difficile) est une espèce de bactérie omniprésente. Les infections à Clostridioides difficile sont l’une des principales causes de diarrhée et de mortalité dans les hôpitaux.
Jusqu’à récemment, l’espèce Clostridium difficile appartenait au genre Clostridium, qui fait partie de la famille des Clostridiacées, ordre des Clostridiales, classe Clostridia et s’appelait Clostridium difficile. Récemment, la place de cette espèce dans la taxonomie des bactéries a changé à plusieurs reprises, elle a été reclassée dans le genre Peptoclostridium, sous le nom de Peptoclostridium difficile, et en 2016 elle a été transférée au genre nouvellement organisé Clostridioides, qui a été inclus dans la famille. Peptostreptococcaceae, du même ordre des Clostridiales et de la classe Clostridia, phylum Firmicutes, <groupe sans rang> groupe des Terrabacteria, royaume des Bactéries et est donc devenu connu sous le nom de Clostridioides difficile (un nom équivalent valide est Clostridium difficile.
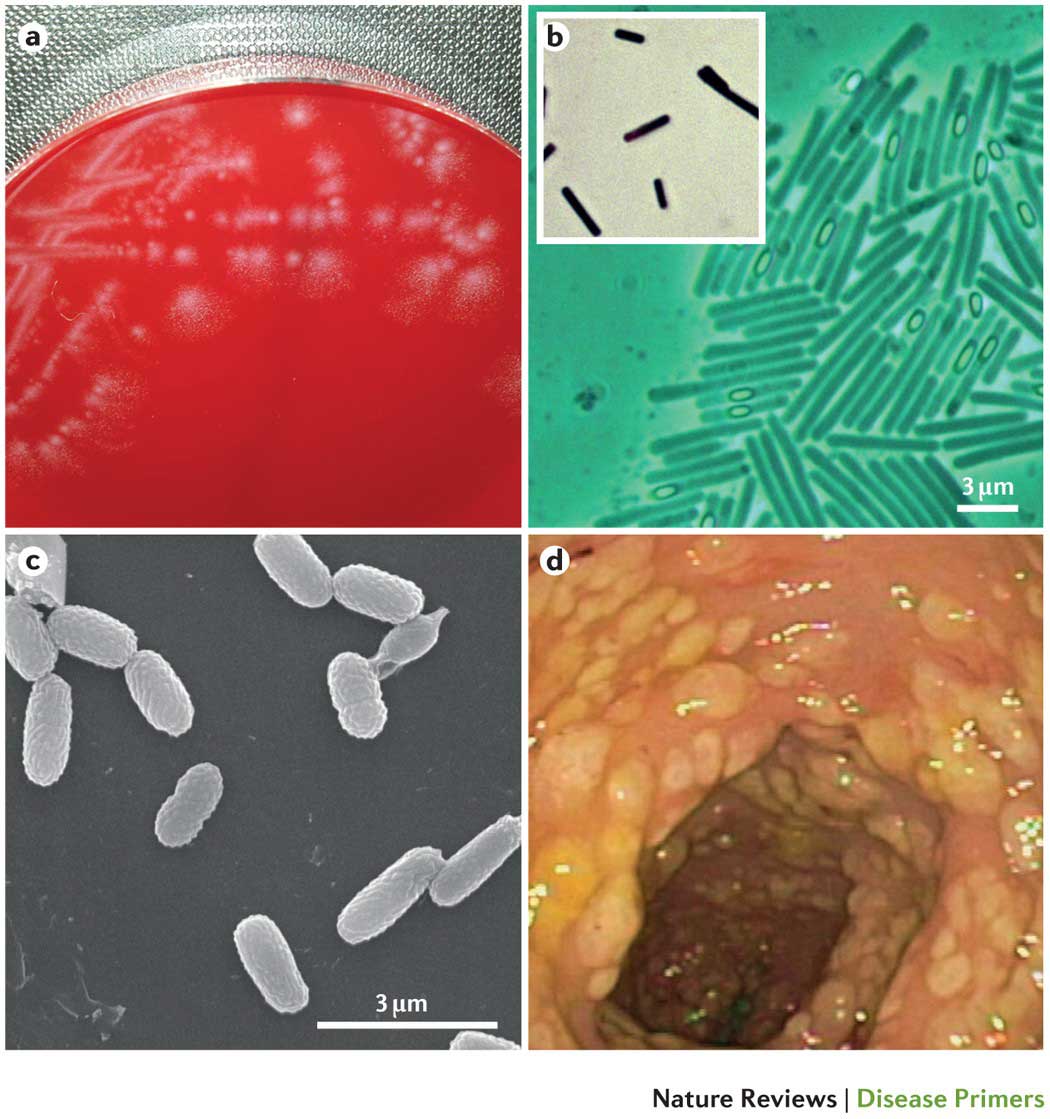
Infection à Clostridium difficile
Clostridioides difficile sont des bactéries Gram positives, sporulées, strictement anaérobies, en forme de gros bâtonnets allongés avec un renflement au milieu. Clostridioides difficile peut survivre longtemps dans l’environnement extérieur. Ses spores résistent au traitement thermique. Clostridioides difficile est naturellement résistant à la plupart des antibiotiques.
Les souches toxigènes de Clostridioides difficile produisent plusieurs facteurs pathogènes. Les plus étudiées d’entre elles sont:
– la toxine A (entérotoxine)
– la toxine B (cytotoxine)
– une protéine qui inhibe la motilité intestinale
Clostridium difficile fait partie de la microflore normale du tractus gastro-intestinal (colonise principalement le gros intestin, mais peut être trouvé dans l’intestin grêle et la cavité buccale) et du tractus génital féminin et, parfois, de la peau. Clostridium difficile est présent dans les intestins d’environ la moitié des nouveau-nés et chez 3 à 15% des enfants de plus de 2 ans et des adultes en bonne santé. La quantité de Clostridium difficile dans la microflore intestinale normale d’un adulte en bonne santé ne dépasse pas 0,01 à 0,001%. Cependant, lors de la prise d’antibiotiques, ce dernier chiffre peut atteindre 15 à 40%.
La diarrhée associée aux antibiotiques (DAA) est l’une des complications qui surviennent chez 5 à 25% des patients prenant des antibiotiques. Clostridium difficile n’est pas la seule cause d’AAD, même s’il est assez fréquent (environ un tiers des cas). L’AAD peut également être causée par Salmonella spp., Clostridium perfringens type A, Staphylococcus aureus, Klebsiella oxytoca, les champignons candida et d’autres micro-organismes. L’AAD fait partie des infections nosocomiales les plus répandues. Rien qu’aux États-Unis, jusqu’à 1 million de cas d’AAD sont enregistrés chaque année. Malgré le portage important de Clostridium difficile, les nourrissons ne souffrent pratiquement pas de DAA causée par Clostridium difficile.
L’apparition de l’AAD est due au fait que les antibiotiques suppriment non seulement la microflore intestinale pathogène, mais également normale, ce qui, dans des conditions normales, empêche la multiplication des micro-organismes pathogènes et opportunistes. En raison de l’effet des antibiotiques sur la microflore normale, le nombre de microbes pathogènes et opportunistes résistants aux médicaments (y compris Clostridium difficile) dans le corps humain peut augmenter considérablement.
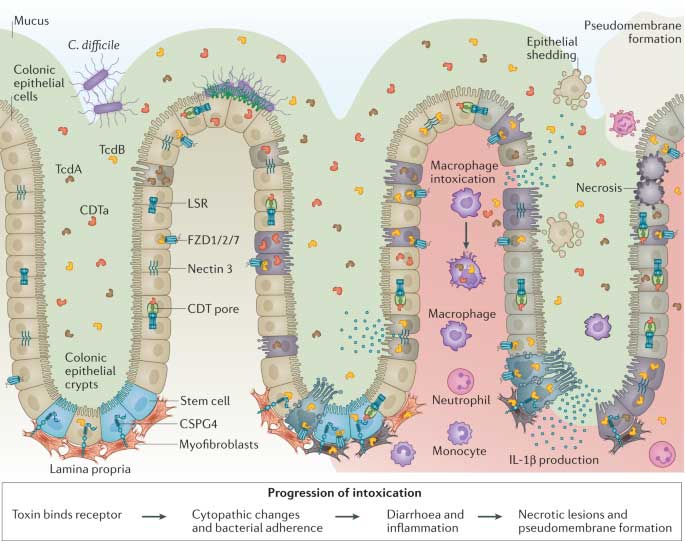
Toxines de Clostridioides difficile : mécanismes d’action et thérapeutiques antitoxines
La cause de l’AAD peut être presque n’importe quel agent antimicrobien, mais l’incidence de la maladie dépend considérablement du type d’antibiotique (et est presque indépendante de la dose). Le plus souvent, l’AAD est causée par la prise de clindamycine, de céphalosporines et d’ampicilline.
Les manifestations de la DAA vont d’une diarrhée légère à une entérocolite sévère appelée «colite pseudomembraneuse». La cause de la colite pseudomembraneuse dans la grande majorité des cas est une infection à Clostridium difficile.
Le principal facteur de risque de survenue de formes sévères d’AAD à Clostridium difficile est l’antibiothérapie. Même une dose unique d’un antibiotique à large spectre, quels que soient la dose et la voie d’administration, peut conduire au développement d’une AAD et d’une colite pseudomembraneuse. Un long séjour hospitalier, notamment dans le même service avec des porteurs de Clostridium difficile, est également un facteur de risque.
La colite pseudomembraneuse se caractérise par une diarrhée aqueuse abondante et fréquente, parfois mêlée de sang, de mucus et de pus. En règle générale, la diarrhée s’accompagne de fièvre, d’une température élevée entre 38,5 et 40°C, de douleurs abdominales modérées ou intenses, de crampes ou de nature constante. Le taux de mortalité en l’absence de traitement chez les patients atteints de colite pseudomembraneuse est de 15 à 30%
Une caractéristique de l’infection à Clostridium difficile est ses rechutes fréquentes – en moyenne 20 à 25%, dont la cause est associée à la présence de spores de Clostridium difficile dans les intestins ou à une réinfection. Habituellement, après le traitement, une guérison ou une amélioration se produit, mais aux jours 2 à 28 (en moyenne 3 à 7 jours), une rechute se produit, identique à l’épisode initial.
Diagnostic et traitement de la DAA causée par Clostridium (Clostridioides) difficile
Les principaux facteurs dommageables pour le corps humain dans les maladies causées par Clostridium difficile sont les toxines A et B. Toutes les souches de Clostridium difficile ne produisent pas ces toxines. Afin de détecter une infection par des souches toxigènes de Clostridium difficile, un test de selles est effectué pour détecter la présence de toxines A et B ou un test de selles – culture pour Clostridium difficile. Normalement, les résultats des tests devraient être négatifs.
Si une AAD est détectée, l’antibiotique à l’origine de la maladie doit être arrêté. Le traitement des cas graves de DAA et de colite pseudomembraneuse comprend un traitement à la vancomycine ou au métronidazole, auxquels la plupart des souches de Clostridium difficile sont sensibles. La prise de médicaments antidiarrhéiques et d’antispasmodiques n’est pas autorisée en raison du risque de développer une complication grave – un mégacôlon toxique.
Un probiotique efficace est Enterol, qui contient des levures lyophilisées Saccharomyces boulardi, qui ont un effet antimicrobien direct non seulement contre Clostridium difficile, mais également contre d’autres micro-organismes pouvant causer l’AAD. Pour prévenir le développement de l’AAD et restaurer la microflore intestinale après l’arrêt d’un antibiotique (vancomycine ou métronidazole), des médicaments contenant des souches de représentants de la microflore naturelle sont utilisés : Lactobacillus acidophilus, Lactobacillus rhamnosus, Bifidobacterium longum, Enterococcus faecium et autres (Linex, Bifiform, etc.).
L’Organisation Mondiale de Gastro-entérologie note l’efficacité de l’utilisation de la souche Lactobacillus casei DN-114 001 pour le traitement de la diarrhée associée à Clostridium difficile, ainsi que pour sa prévention, les souches probiotiques suivantes (Probiotiques et prébiotiques. Recommandations pratiques):
– Lactobacillus casei DN-114 001 dans du lait fermenté avec Lactobacillus bulgaricus et Streptococcus thermophilus 1010 Cfu, 2 fois par jour
– Lactobacillus acidophilus + Bifidobacterium bifidum (souches spéciales) – 2 x 1010 Cfu chacun, 1 fois par jour
– Saccharomyces cerevisiae (boulardii). Âge 1 an – 2 x 1010 Cfu par jour
– Oligofructose – 4 g, 3 fois par jour, 4 g.
Agents antibactériens actifs contre Clostridium difficile : vancomycine, métronidazole, rifaximine, tétracycline, doxycycline, lincomycine. Clostridium difficile est résistant à la ciprofloxacine. Le 21 octobre 2016, la FDA américaine a approuvé l’utilisation aux États-Unis d’un nouveau médicament destiné à prévenir les rechutes de l’infection à Clostridium difficile chez les patients de plus de 18 ans – le bezlotoxumab, nom commercial Zinplava. Le bezlotoxumab est un anticorps monoclonal conçu pour neutraliser la toxine B de Clostridium difficile.